化妆品安全评估基础数据分析和挑战探讨 - 李锦聪
摘要:依据化妆品安全评估报告简化版和完整版可采用的评估证据要求,对《已使用化妆品原料目录(2021版)》的8972种原料与《化妆品安全技术规范(2015版)》、权威机构的评估结论(WHO/FAO/CIR/GRAS/SCCS/IFRA)等相关数据搜集整理、统计分析。讨论了化妆品新规实施和目前简化版安全评估行业面临的专业人才缺乏以及未来完整版安全评估可采用证据缺口大等问题给行业带来的影响,并对现行法规实施带来的影响提出了相应的政策过渡方案与分阶实施等意见。
1 化妆品安全评估报告面临的问题
为贯彻落实《化妆品监督管理条例》,规范和指导化妆品安全评估工作,国家药监局发布了《化妆品安全评估技术导则(2021年版)》(以下称《安评导则》),自2021年5月1日起施行。导则规定自2022年1月1日起,化妆品注册人、备案人申请特殊化妆品注册或者进行普通化妆品备案前,必须依据《安评导则》的要求开展化妆品安全评估。导则同时要求2024年5月1日前,化妆品注册人、备案人可以按照《安评导则》的要求开展化妆品安全评估,提交产品安全评估资料。因此,化妆品安全评估报告(CPSR)成为化妆品产品注册备案中不可缺少的一部分。目前,在简化版安全评估报告中,涉及主要评估证据包括以下:
此外,从2024年5月1日起,化妆品注册备案时需要提交化妆品完整版的安全评估报告,且不能再使用前述的第(三)、(四)条作为评估证据,这一时间节点和证据排除要求对于当前行业实施完整版安全评估报告构成了不小的困难。
2 简化版安全评估数据基本情况
2.1 《化妆品安全技术规范》
在《已使用化妆品原料目录》中《化妆品安全技术规范》共有723种相关原料包括化妆品限用组分、准用防腐剂、防晒剂、染发剂、着色剂,其中,有限值要求原料约350种,无限值要求原料约350种,剩下部分属于规范类别统称不在计算范围内。另外,还有54种原料被禁止在化妆品中使用。然而,对于《化妆品安全技术规范》中无限值要求的原料,目前《安评导则》没有明确具体的评估要求。这导致企业在使用这约350种原料时,缺乏可供参考的安全浓度/限值,这是否意味着这350种原料在任何使用量下都是安全的吗?答案是不一定的,还需要监管部门进一步明确相关要求。
根据《化妆品监督管理条例》中对化妆品原料按风险程度分级管理的规定,《化妆品安全技术规范》中的原料属于高风险原料,按注册管理。除了部分在各国法规中有明确限值或者国际权威机构已经给出安全使用结论的原料外,对于《化妆品安全技术规范》中其他无限值要求的原料,企业的安全评估人员在评估这类原料时将面临极大的证据采用困难,其评估结论面临是否采信的风险。
2.2 《已使用化妆品原料目录(2021版)》
根据《已使用化妆品原料目录》,按目录中的驻留类和淋洗类进行分类和数据统计,同时将植物来源的相关原料也进行了人工筛查统计分析,得出有最高历史使用量的分别为驻留类产品5906种,淋洗类产品2434种,通过对驻留和淋洗重叠的原料进行删除处理,有最高历史使用量数据的原料共计6492种。其中,植物来源相关原料约3600种,占《目录》总比的40%。
具体而言,《已使用化妆品原料目录》能用于化妆品安全评估的数据共有6492种,加上《化妆品安全技术规范》相关的限用、准用原料约700种,两种评估证据相关原料共计7192种,也就说还有1780种原料需要找其他类型证据作为补充。此外《已使用化妆品原料目录》中虽有最高历史使用量,但该使用浓度远低于研发人员选用该原料需要实际使用浓度的组分不在少数。7192种原料的最高历史使用量证据并非完全具有使用价值,实际可用原料范围会进一步缩小。
2.3 权威机构评估结论(CIR)的数据
以权威性和数据量最多的CIR数据为例,通过长达一年多的人工检索搜集,将我国《已使用化妆品原料目录》相关的原料数据与已搜集到的CIR数据进行INCI名称匹配,对两者相关的每个原料作进一步统计分析。
根据美国化妆品原料评价委员会(CIR)网站公开发布的评估数据,结合我国《已使用化妆品原料目录》的8972种原料以INCI英文名称在CIR网站中进行逐一检索和搜集,结果显示,CIR网站上能找到3325种化妆品原料与我国已使用化妆品原料目录相关的数据。同时CIR报告中的数据与我国《已使用化妆品原料目录》最高历史使用量相似,部分原料CIR评估结果中给出了相应的安全使用浓度。其中,驻留类产品相关的有1774种和淋洗类产品相关的有1534种。此外,还有1337种原料CIR未提供安全使用浓度数据。再进一步将驻留类和淋洗类数据,通过原料名称进行去重复处理,得到了1948种有安全使用浓度数据的原料,如此看来CIR数据库中也仅有1948种原料的安全数据可供我国开展化妆品安全评估时作为证据。
2.4 简化版三种评估证据类型总结分析
综上所述,在《化妆品安全技术规范》数据中,可使用化妆品的原料约700种,在《已使用化妆品原料目录》数据中,有最高历史使用量的原料共计6492种,在CIR数据中,有安全使用浓度的原料共计1948种。其中《已使用化妆品原料目录》与CIR数据存在重叠情况,将两组数据比对后,其中有1813种重叠的,这样可以看出经过整理CIR数据中有135种原料可以用于弥补《已使用化妆品原料目录》无最高历史使用量的。最终得到的数据为:
有最高历史使用量或安全使用浓度,可以用于化妆品简化版安全评估的数据共约6492(原料目录)+700(技术规范)+135(CIR补充)=7327种;
无最高历史使用量或安全使用浓度,需要进一步检索其他权威机构评估结论或者需要找毒理学终点及加测毒理学试验获取新证据的原料共计8972(原料目录)-7327(有数据含规范无限值)-54(禁用原料)=1591(简化版无证据和数据)。
2.5 简化版安全评估报告面临的困境
化妆品安全评估对人员要求高,就目前而言,根据“广东省化妆品科学技术研究会”2023年5月初步调查统计结果显示,目前能自主完成简化版安全评估的企业仅占17%,仍有82.9%无法自主完成简化版安全评估报告。
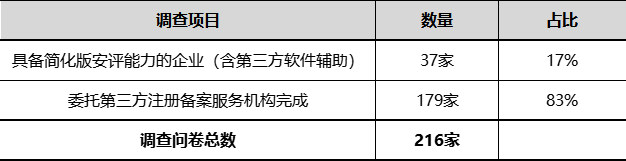
原因可能包含以下几点:
1)由于负责安全评估的人员能力知识水平不足,导致报告撰写时间过长,人力成本增加,因此企业老板选择放弃自主评估;2)为了提高安全评估人员工作效率,企业选择购买第三方平台软件作为辅助工具;3)相对自主评估费用第三方注册备案服务机构出具的评估报告费用更为低廉;4)评估人员虽然具备简化版评估能力,但日常工作量已经饱和,没有多余时间用于安全评估工作。此外,由于评估人员经常遇到无简化版评估证据的原料,因此选择第三方机构更为省事。
1)实际配方中原料的添加浓度超过《已使用化妆品原料目录》中的最高历史使用量或权威机构评估结果的安全用量;2)仅有淋洗类而缺失驻留类数据,实际工作中会遇到配方中使用的部分原料,在现有的数据中无法找到相对应的驻留类产品最高历史使用量或权威机构评估结果的安全用量;3)原料供应商无法提供完整的原料安全相关信息或者安全评估结论,同时其他证据的数据又缺失,需要另外送检加测毒理学试验,大大增加了新品的开发周期和昂贵的检测费用,最终可能选择弃用该原料。4)企业为避免安评证据缺失,而将原料选用范围缩小到CIR有数据库范围内或者已使用化妆品原料目录有历史最高记录的原料范围以内,这导致更为严重的产品同质化。
3.1完整版安评原料已有证据状况
距离2024年5月1日起实施完整版安全评估只剩下几个月的时间,根据《安评导则》和现有数据,对完整版安全评估的整体情况进行分析,评估数据主要有《化妆品安全技术规范》中限用组分和准用防腐剂、防晒剂、染发剂、着色剂原料,以及国际主流权威机构的评估结论WHO/FAO/CIR/GRAS/SCCS/IFRA等安全使用量。
不详细列出具体数值,总体而言根据我个人所搜集的数据来看,其中国际主流权威机构得到的数据约为2600(含CIR的1948),另这个数据中有部分与《化妆品安全技术规范》有重叠,很多数据还需要人工分类对应原来目录以及种种原因,情况分析起来较为复杂,所以选择不公开具体数据。技术规范和国际主流数据结合去重后得到的数据约为:3200,这已经是非常保守的数据。
根据世界各国法规和权威机构公开发表数据,部分数据已经对化妆品原料在使用时提供了限值要求,剩下部分的原料在安全评估过程需结合配方中实际使用情况进行分析。除了有明确限值要求外,无限值的部分可以通过加测或检索局部毒理学终点来证明该原料可安全使用于化妆品,通常这部分的原料在无限值的情况下是可以豁免系统毒性来降低完整版安全评估的难度和毒理学试验成本。
3.2 植物来源相关原料数据
此外,通过上述数据中了解到在《已使用化妆品原料目录》中,植物来源相关原料约有3600种,占总比的40%,我们对3600种植物来源的原料,结合我国政府部门公开发布的相关通告和标准等数据(可食用、药食同源、保健品、历史悠久、美国草药BOTANICAL SAFETY HANDBOOK等)作为评估证据,通过搜集、分类、筛查等工作。
这几个可食用相关分类数据与技术规范和国际主流权威数据比对,也存在重叠情况,经去重后,综合后得到的约为4000,这也是非常保守的数据。其中关于无限值的原料,还需近一步进行局部毒性试验来证明其安全性,但如果真能豁免系统毒性试验,个人经验分析这也已经非常好了。
3.3 完整版安评数据总体情况分析
《已使用化妆品原料目录》共计8972种原料,以最好的分析情况来看,约4000种原料评估起来相对容易的,但只占了总比的45%,剩下的5000种(55%)的原料需要进行完整版安评(危害识别、剂量反应关系评估、暴露评估、风险特征描述)既按照《安评导则》要求需要对全部毒理学终点进行评估,化妆品安全评估局部毒性和系统毒性试验主要有:
剩下的5000种(55%)化妆品原料的完整版评估,还可以结合欧洲化学品管理局(ECHA)等数据库进行毒理学终点搜集,从而进一步解决评估难题。因为ECHA网站的数据搜集和分析都需要人工逐一检索,不管是搜集难度还是数据结果分析,对于评估人员的要求都非常高,所以不对这部分数据统计分析。
3.4 完整版安评主要履职人基础状况
结合实践经验来看,具有完整版化妆品安全评估能力的人,至少要符合《安评导则》要求,符合该要求的或者同等水平的人几乎接近毒理学家水平。为此,我们在中国毒理学会(CST)网站中找出2015-2022年通过考试认证的毒理学家名单数据,共计481人,其中化妆品企业或品牌相关的共计39人,详情见下表:
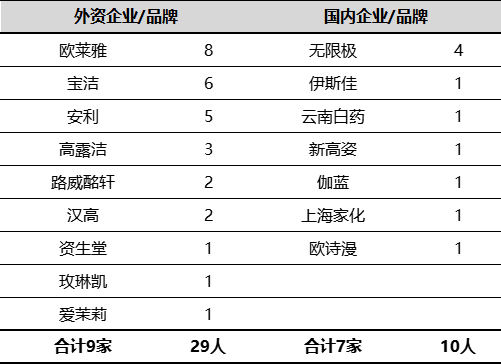
此外,根据另一项关于化妆品质量安全负责人的专业调查报告结果显示,具有毒理相关专业数据为0,化工相关专业为165,占比76.4%,统计结果见下表:
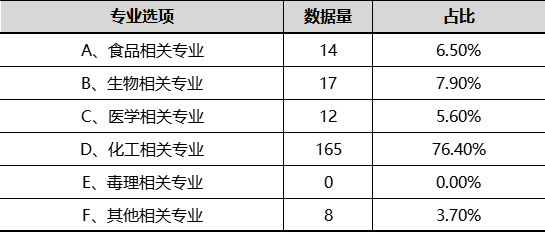
由此可知完整版安全评估,当前行业严重缺乏相应专业人才和评估数据缺口较大,对行业来说是一个极大的挑战。
3.5 完整版安评行业使用频次最高的原料数据分析
几乎能静下心来分析8972种已使用原料所有安评相关数据的人士应该屈指可数,我算其中一个吧,可能大部分的安评人,只是对本企业所涉及的一千几百种原料更为关心,也无法操心这个行业的情况。工作中已经非常忙,相信也没有企业愿意自己的员工为行业无私奉献。
通过几轮的数据分析后,可能大家对这些数据还是没有一个完整的概念,到底对行业影响有多大程度?所以,我特意在美丽修行大数据平台进行人工检索排序,以及需求了数美链大数据平台的帮助。对另一组核心数据进行了最后的分析总结,也是我个人认为最难、最担心的。
因此,我以2017年5月至2023年5月在我国境内已注册备案的化妆品,5的数据作为统计区间,筛选出整体使用频次最高TOP500原料以及使用频次最高的活性TOP500原料排行榜单,进行了更具有统计意义的分析:
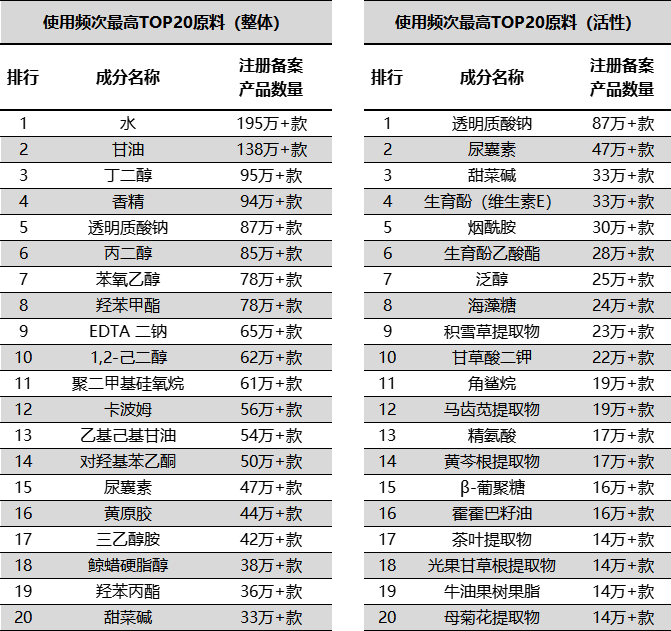
(由于篇幅限制,仅展示部分数据,数据来源:数美链)
行业使用频次最高的原料的完整版安评数据情况,很大程度上反映了行业整体,因为涉及的配方也相当多。如果这些我们常用的原料都缺乏安全用量或限值等有力的证据,也说明了完整版安评对行业带来的影响有多大。
最终排除多种不确定因素,就以数据量最大的《化妆品安全技术规范》和“权威机构CIR评估结论”对两组TOP500原料进一步分析,统计结果如下表:
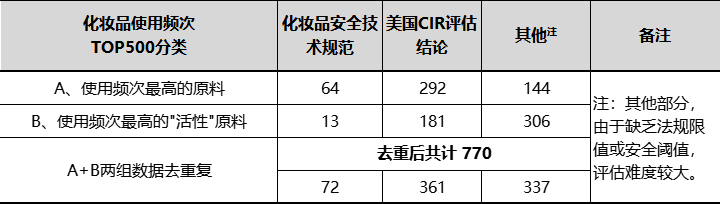
通过上图数据可知,两组使用频次最高TOP500的原料,去重后共计:770种。其中,仍有337种原料缺少技术规范和CIR的数据。熟悉或长期从事化妆品安全评估的人员都非常清楚,CIR数据对完整版安评来说有多重要,缺乏CIR数据,基本可以判定需要进行完整版评估了。就目前我国注册备案已经超过百万级,原料登记报送公示数据也超过了40万。
3.6 完整版安全评估毒理试验数据分析
从上述完整版安全评估数据得知,至少还有5000(占总比55%)的原料需要进一步的数据搜集或者原料和终产品加测毒理学试验来补充数据缺口。为此,我们对目前毒理学试验方法、周期、动物数量、参考费用做了另一项统计:
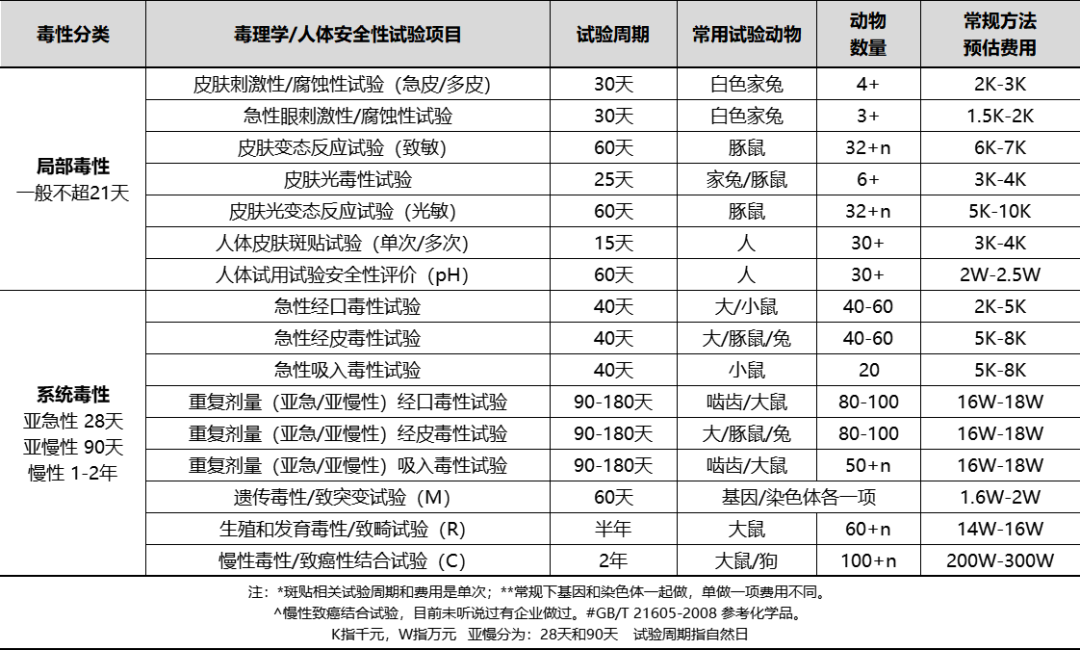
未来面临完整版安全评估,约5000种原料需要找到相关毒理学终点,根据目前安全评估实践经验来看,大部分原料毒理学终点来自化学品行业,而化学品行业的原料虽多但与化妆品原料重叠的只有一部分。此外,化学品行业的局部毒性存在缺失,并不像化妆品行业这样,工作中发现化学品行业的通常会做急性经口或经皮和皮肤刺激性、眼刺激性较多,未涵盖化妆品行业的其他局部毒性如:皮肤变态反应、皮肤光毒性和光变态反应试验。
目前很多原料商提供的原料毒理报告,观察发现原料商只选择做急性经口或经皮和一项刺激性试验试验项目,而且部分试验项目采用的试验方法非《化妆品安全技术规范》和国家、行业相关的标准方法,存在科学性、合规性等问题,他们只做了某一项毒理试验就认为做了“毒理”是安全的,主要原因可能是此前化妆品法规没有硬性规定,另急性试验费用相对较低,实际安全评估中反而对重复剂量亚慢性试验(28天LOAEL/90天NOAEL)数据需求更大,因为有了LOAELAEL值,可以用于计算安全边际值(MoS)。
鉴于目前我国化妆品新规实施不久,不管是化妆品生产企业还是化妆品相关原料商,仍需要不断地学习和实践,充分了解化妆品相关安全评估需要提供的证据和资料还需要时间、资源的筹备和再投入。
目前,《安评导则》未对《已使用化妆品原料目录》的原料进行规定,难度堪比新原料评估还要大,新原料至少有情形1至情形6来指导,什么原料该如何选择哪些毒理学试验。同时,已使用也没有明确哪些原料在无数据或无法找到毒理学终点时,该如何选择毒理学试验项目,很多评估人员也经常提出是不是全部毒理都要评估或加测,这种情况是目前评估人员比较困惑的。
4 化妆品安全评估进展探讨
当前化妆品安全评估面临人才短缺、经济整体环境欠佳、经营困难、法规改革深入纵深、评估数据缺口和系统毒性试验资源等挑战。为解决问题,建议延长简化版过渡期、制定相应的新政策解决缺乏数据的原料评估、设定浓度豁免系统毒性试验等指导性规范文件,保持条例设定的方向不动摇,调整法规落地的力度和节奏,并分阶段实施,以促进行业健康高质量发展和高水平规范化经营。
4.1 安评相关专业人才短缺
行业缺乏专业人才是一个根本性问题。进行化妆品安全评估需要具备医学、药学、生物学、化学或毒理学等相关专业知识,并且必须有5年以上的从业经历。然而,要完整彻底的履职其能力要求远超任职资格要求,因此,专业人才的短缺导致了安全评估工作的实施困难,企业无法自主完成化妆品安全评估工作。
监管部门应给予企业更多时间对相关人才培养和引进,政府和行业协会、高校应多组织开展交流和合作,尤其是高校应该增强化妆品安评相关课程的建设,为行业供应符合产业需求的专业人才;各方应当加强对安全评估人员的的教育培训,提高安全评估人员的专业知识和技能,增强安全评估能力,共同解决安全评估人才眼前短缺的突出问题,维护条例尊严,高水平促进行业的发展。
4.2 新规30年大改革
2021年1月1日随着《化妆品监督管理条例》的正式实施,化妆品法规大改革给行业带来了新的希望的同时也带来许多新的挑战。从业者需要花费更多的时间去学习新规,并且了解、理解和执行新规。此外,已经注册备案的产品需要不断进行整改以符合新规定,这包括产品配方的调整、包材的更换等,从而导致一个产品可能存在多个版本的包材。这些问题加上疫情的影响导致的销售业绩不佳,大量库存积压,企业需要更多时间来消耗库存,实现经营资金的回流。
化妆品企业需要逐步进行整改,确保产品符合新规定的要求,同时避免过度整改浪费资源和时间。综合考虑市场需求、竞争状况、消费者偏好等因素,并制定相应的销售策略来推动库存消耗和提升业绩。寻找多元化发展的可能性,开发新产品、拓展新渠道、探索新市场等方式,寻找增长点和创新机会,为企业的发展提供动力,只有经营状况好转新规约定的高要求才有资金投入、人员更新和补充。
4.3 完整版安评可采用现成证据缺口大
2024年5月1日起实施完整版安全评估,据调查分析结果显示,完整版安全评估报告有约5000种的原料需要通过搜集毒理学终点或加测毒理学试验来完成安全评估,大大增加了新品上市的时间和成本。此外,自从实施简化版安全评估以后,现有的配方都是基于目前的简化版评估数据而开发的,到了完整版以后,现有的原料如果无法完成获取完整版评估证据,将导致许多企业不得不弃用这部分原料,造成大量无法安全评估的原料被淘汰报废处理,无疑又增加企业经营的成本。
建议将《已使用化妆品原料目录》的最高历史使用量以及本企业原料历史使用量的简化版评估证据分阶实施,再给予企业2-3年缓冲过渡期。具体措施是将《已使用化妆品原料目录》最高历史使用量的延长期限至2026年1月1日,并将已经报送过的各企业原料历史使用量再一次汇总结合CIR等国际权威机构当前的安全评估结论,用于更新《化妆品已使用原料目录》供企业使用。
当前,我国已成为世界上第二大化妆品消费市场。我国在短短30年就已经赶上国际上欧美国家等地区的上百年历史的监管模式,并完善了全部普通化妆品网上注册备案、配方真实浓度披露,取得了非常好的改革成就。延长实施完整安全评估报告过渡方案的分析考虑了我国化妆品产业的发展现状和国际趋势。在新规实施之前,国内普通化妆品未规定需要填报全部原料的浓度,如在现施行的简化版评估结论为安全的或局部毒性试验结果为安全的基础上,虽然过渡期内存在一定的风险性,但随着我国化妆品不良反应监测不断完善结合已注册备案的化妆品原料在化妆品使用的真实浓度,在未来几年可以逐步建立起国内化妆品不良反应与原料使用的大数据,进一步提高化妆品安全性的评估和监管水平。
同时,随着国际上禁止动物测试的趋势,我国在积累大量化妆品原料真实使用浓度在人体上的“临床”数据后,可以依据毒理学角度来对化妆品进行安全评估。人体临床数据相对动物实验更真实可靠,且可提供更准确的原料安全最高使用量。随着禁用、限用、准用原料的检定方法和动物替代方法不断完善,我国将通过不良反应监测、化妆品注册备案数据以及参考国际权威机构的限值和安全评估结论,形成一套与国际水平相当的化妆品安全技术规范和已使用化妆品原料目录。
总的而言,这样的分阶实施和过渡措施是一个有利于行业发展和提升化妆品安全评估水平的举措。给予企业和安全评估人员更多时间来进行完整版评估学习和筹备,减轻他们的压力。并为本企业原料历史使用量争取更多时间,避免大量原料的浪费和报废处理,减少企业经营成本的增加,提高安全评估和配方与原料更替的可操作性。同时,将减少对动物试验的依赖和负担,提高化妆品安全评估的可靠性。
通过采用更先进的评估方法和现有真实数据进行评估,我国将逐步实现与国际水平相当的化妆品安全评估体系,为消费者提供更安全、可靠的化妆品。此外,这个过渡期也给予全国高校开展化妆品相关领域的研究和专业人才培养的周期,通过适当的教育和培训,新生力量可以在大学期间就接受相关知识和技能的培养,这将使他们毕业后能够迅速适应行业的需求,为化妆品行业的发展和创新做出积极贡献。有助于为化妆品行业提供更多高素质的人才支持,推动行业的高质量发展。对于从业人员来说2021年至2026年,这5年时间给他们继续学习实践的周期,这也真正意义上符合《安评导则》所说的5年相关工作经验的条件。
4.4 系统毒性试验问题
完整版实施以后,由于约5000种原料缺乏法规限值和权威机构结论安全使用量,需要进一步的评估其安全性,评估安全性涉及毒理学,毒理学中最难解决的是生殖发育、亚慢性试验以及慢性致癌结合试验。系统毒性试验的周期长和费用高昂确实给企业带来了困扰。这导致许多企业不得不弃用这部分原料,从而减少了可评估的原料数量。这种情况下,化妆品行业可能面临产品同质化和创新不足的问题,对行业的高质量发展不利。
建议出台相关政策,解决无安评数据的原料的评估问题。具体措施可以包括考虑采用《新原料注册备案资料管理规定》的情形1至情形6作为评估依据,就算遇到没有法规限值或权威机构安全使用量的原料,如法规能提供明确的“毒理学试验项目”选择,企业评估人员可按不同原料特性进行分类,然后再选择相应的“毒理学试验”进行加测,从而减少安全评估以及毒理学试验的周期和费用,降低企业的难度。
对于含量较低且缺乏系统毒理学研究数据的原料,根据《安评导则》规定,可参考使用毒理学关注阈值(TTC)方法进行评估,但也建立在非遗传毒性物质基础上,排除遗传毒性的成本也不低。另外,对于缺乏系统毒理学研究数据的非功效成分或风险物质,可参考使用分组/交叉参照(Grouping/Read Across)进行评估,各方意见和评价不统一,评估难度也极高。建议尽快出台我国的TTC以及分组/交叉参照评估方法指南,方便安全评估人员阅读理解和执行,当然这些分类处理的临时措施也可以设置过渡期。
对于含量较低且缺乏系统毒理学研究数据的原料,而在实际工作中观察发现,有很多原料属于概念添加,法规又未明确添加浓度的下限值,有些原料在配方中实际添加浓度已经是ppm或ppb级别,但根据法规要求企业又不得不对其进行安全评估,又遇到系统毒性带来的问题。是否可以制定相应的规定进一步细化,当原料在配方中浓度低于多少可以豁免安全评估或者说系统毒性,比如:原料在配方中添加的浓度在1ppm以下。
4.5.毒理试验数据与报告
在化妆品安全评估实践与交流中,遇到关于同一注册备案人或生产企业在相同产品配方、产类型和使用方法以及同一个原料和供应商等等的前提下,是否能互相参照毒理学数据与报告问题。例如:某个注册备案人,使用某个原料在A产品添加浓度为1%,注册备案时A产品对多项毒理学试验进行了检测,结果显示为合格或阴性。B产品在与A产品完全相同的配方和浓度等一致前提下,是否能采用A产品的安全评估结论作为B产品的安全评估结论依据。当前部分系统毒性,例如生殖发育、急性、亚慢、慢性毒理试验都无法用动物替代,《化妆品安全技术规范》中的方法大部分是针对化妆品“原料”而不是终产品的,实际中还有很多复配原料的问题。因为国外的系统毒性一般针对单一组分的,对于类似复配原料或配方来说,试验结果,也存在非常大的争议。
相关情形案例比较多不一一列举,化妆品安全评估是一项非常重要的工作,法规实施过程遇到很多问题和困难,如何在安全和合规的前提下,行业需要更多法规实施细则来明确相关事宜,避免造成资源过度浪费,减轻合规负担,政策的科学性、合理性也将会进一步加快行业高质量发展。
5 总结
化妆品的安全性报告是对化妆品安全性的全面总结和后期上市后评估的重要参考资料,自2022年实施以来,化妆品行业大部分从业者首次接触这一评估要求,需要了解涉及产品和原料的安全性、评估方法、毒理学试验和数据搜集等方面的知识。原料的限值和安全使用量是安全评估的重要数据来源。然而,完整版评估即将实施,企业需要更长时间过渡适应。同时,现有的评估数据缺口较大,需要制定相应的政策法规和替代试验、评估方法指南来指导,以减少对动物实验的依赖并降低企业经营成本。化妆品安全评估人员需要加强相关知识的学习和实践,以满足完整版实施的要求。
扫描二维码推送至手机访问。
版权声明:本文由化妆品原料网发布,如需转载请注明出处。




