当前位置:首页 > 搜索 "最"
《化妆品风险物质识别与评估技术指导原则》
最大含量50mg/kg;存放于无亚硝酸盐的容器内。2.仲链烷胺、亚硝胺:配方中含有三链烷胺、三链烷醇胺及它们的盐类如三乙醇胺等,或含有单链烷胺、单链烷醇胺及它们的盐类如氨丁三醇、氨甲基丙醇、吡罗克酮乙醇胺盐、乙醇胺等原料时,需要识别并评估....
《化妆品安全评估资料提交指南》
最新暴露量数据或公开发表的化妆品暴露量相关研究文献中的数据;如无公开发表数据的,可基于对产品实际用量的测试和统计结果,评估产品日均使用量,如可采用企业进行消费者试验和调研统计的有效数据等。3.产品驻留因子应根据产品类型、产品特点、产品使用方...
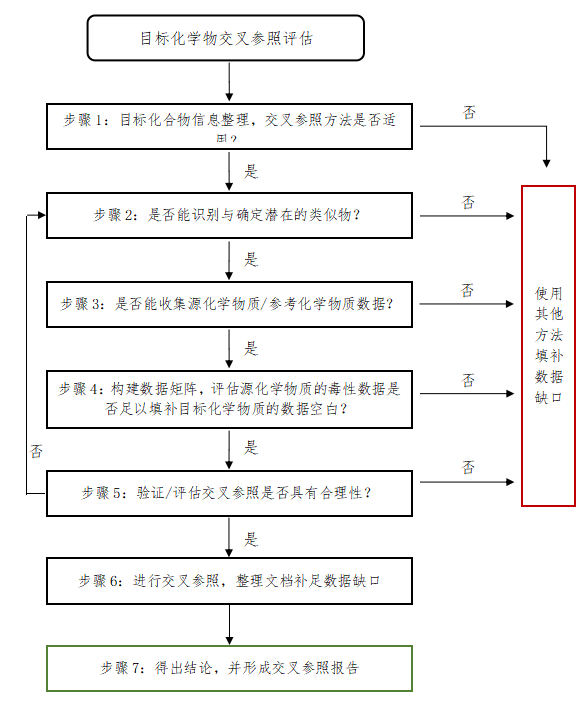
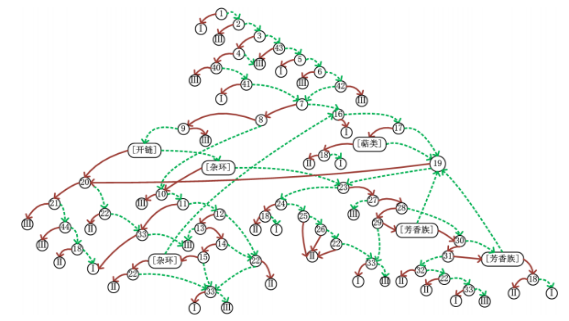
《交叉参照(Read-across)方法应用技术指南》
最后的数据选择合理性进行说明。如果认定对目标化学物质使用交叉参照缺乏合理性,需要使用其他方法填补数据缺口。步骤七:得出结论并形成报告通过以上工作,形成严谨、可信、准确的交叉参照评估报告。报告应包括支持交叉参照的要素,例如目标化学物质和源化学...
《毒理学关注阈值(TTC)方法应用技术指南》
最低的CramerIII类别对比。未知成分在产品中的暴露量为:SED = 1.54×106×1.00×0.1%×8.16%×100%÷60=2.09 µg/kgbw/day,低于2.3µg/kgbw/d......
《化妆品原料数据使用指南》问答
最相关和可靠的数据类型开展评估。二、如何正确应用主要的原料数据类型(三)?世界卫生组织(WHO)、联合国粮农组织(FAO)以及其他国际权威组织,针对食品、食品添加剂和化学品使用等,发布每日允许摄入量(ADI)、每日耐受剂量(TDI)、参考剂...
《国际权威化妆品安全评估数据索引》问答
最新的评估报告为准,并对相关资料进行分析,在符合我国化妆品相关法规要求的情况下,可采用相关评估结论。不同机构评估结果不一致时,根据数据可靠性和相关性,科学合理地采用相关评估结论。......
对《化妆品风险物质识别与评估技术指导原则》的认识和思考
最新要求《技术指导原则》中列出的需要识别与评估的风险物质主要为《技术规范》中的禁用组分,在评估中如果《技术规范》有限量要求的如二噁烷、甲醇等,应符合《技术规范》的相关要求;如果《技术规范》没有限量要求的如二甘醇、苯酚等,可参照权威机构的评估...
中检院关于公开征求《权威机构化妆品安全评估数据索引》等意见的通知
最新的评估结论为主。序号《已使用化妆品原料目录(2021年版)》中的原料序号中文名称INCI名称/英文名称备注1000011-(3,4-二甲氧基苯基)-4,4-二甲基-1,3-戊二酮1-(3,4-DIMETHOXYPHENYL)-4,4-D...
中检院关于发布《化妆品安全评估资料提交指南(征求意见稿)》的通知
最新暴露量数据或公开发表的化妆品暴露量相关研究文献中的数据;如无公开发表数据的,可基于对产品实际用量的测试和统计结果,评估产品日均使用量,如可采用企业自主进行消费者试验和调研统计的有效数据等。3.产品驻留因子应根据产品类型、产品特点、产品使...
中检院关于发布《化妆品风险物质识别与评估技术指导原则 (征求意见稿)》的通知
最大含量50mg/kg;存放于无亚硝酸盐的容器内。2.仲链烷胺、亚硝胺:配方中含有三链烷胺、三链烷醇胺及它们的盐类如三乙醇胺等,或含有单链烷胺、单链烷醇胺及它们的盐类如氨丁三醇、氨甲基丙醇、吡罗克酮乙醇胺盐、乙醇胺等原料时,需要识别并评.....