化妆品原料《体外皮肤变态反应 U937细胞激活试验》潜在致敏性的评价(征求意见稿)
体外皮肤变态反应 U937细胞激活试验
U937 cell line activation Test
(征求意见稿)
1 范围
本方法规定了体外皮肤变态反应 U937细胞激活试验的基本原则、要求和方法。
本方法适用于化妆品用化学原料潜在致敏性的评价。
2 试验目的
本试验用于检测体外培养的人组织细胞淋巴瘤细胞表面标记物CD86的表达,以评价受试物引起皮肤变态反应的可能性。
3 定义
3.1 70%细胞存活率浓度值 70% cell viability(CV70)
受试物染毒后,细胞存活率为70%时对应的受试物浓度值。
3.2 刺激指数 stimulation index(S.I.)
与溶剂对照相比,扣除同型对照后流式细胞仪测定的受试物阳性细胞相对强度值。
3.3 CD86有效作用浓度值 Effective Concentration 150(EC150)
CD86的相对荧光强度值达到150时对应的受试物浓度值。
4 试验的基本原则
当致敏物质接触皮肤后,树突状细胞在移动到淋巴器官的过程中分化成熟,并上调一系列表面分子的表达。体外培养类树突状细胞:人组织细胞淋巴瘤细胞,并和受试物共暴露48h后,使用荧光抗体染料对细胞表面分子CD86染色并用流式细胞仪测定,从而评价受试物是否具有致敏性。
5 试剂
5.1 细胞
选用人组织细胞淋巴瘤细胞(The human histiocytic lymphoma cell line,U937细胞)。细胞使用前应进行稳定性检测。推荐使用clone CRL1593.2细胞株。
5.2 培养基
RPMI 1640基础培养液中加入10%胎牛血清、适量抗生素,配制成1640完全培养基。
5.3 染色缓冲液
磷酸盐缓冲液中加入5%的胎牛血清。
5.4 染料和抗体类物质
7-氨基放线素菌-D染料(7-AAD)
FITC标记的小鼠单克隆CD86抗体(FITC-CD86)
FITC标记的小鼠IgG1(FITC- IgG1)
6 试验方法
6.1 细胞准备
6.1.1 细胞培养
U937悬浮细胞使用1640完全培养基,于37℃、5%CO2培养箱内培养,倒置显微镜下观察细胞状态。细胞复苏一周并通过稳定性检测后可开展试验。细胞最大培养浓度不超过2×106个/ mL,复苏后使用不超过6周,传代次数不超过21代。
6.1.2 细胞稳定性检测
细胞复苏两周后,选用松香酸(AA)或2,4,6-三硝基苯磺酸作为阳性对照,乳酸(LA)作为阴性对照。当细胞可以准确对阳性物质和阴性物质进行稳定区分时视为通过稳定性检测。
6.2 受试物处理
溶剂:完全培养基(优先选择)或二甲基亚砜(DMSO)
受试物储备液:第一次运行至少选择6个浓度。于试验前一天制备,应用1640完全培养基配制0.4 mg/mL的受试物溶液,或者应用DMSO配制50 mg/mL的受试物溶液。由于没有进行剂量测定,因此在第一次运行时,应在相应的溶剂中配制6种系列浓度储备液(最终浓度为1、10、20、50、100和200µg/mL)。
受试物工作液:于试验当天制备,用完全培养基配制的受试物溶液可以直接使用,用DMSO配制的受试物溶液需用完全培养基稀释125倍得到工作溶液。将工作液等体积加入细胞悬液中进行染毒,即最终细胞接触浓度是工作液浓度再稀释2倍。
连续运行的浓度选择:基于第一次运行的结果选择至少4个第二次运行的浓度,任何后续运行的浓度都是基于之前所有运行的单个结果来选择。由于浓度间隔设置较小会影响浓度效应,所以建议以下推荐使用的最终浓度(单位:µg/mL)进行试验: 1 – 2 – 3 – 4 – 5 – 7.5 – 10 – 12.5 –15 –20 – 25 – 30 – 35 – 40 – 45 – 50 –60 – 70 – 80 – 90 – 100 – 120 – 140 – 160 – 180 – 200。
如果以上浓度无法测得受试物的70%细胞存活率浓度值(70% cell viability,CV70),可以进行浓度调整。但受试物最终细胞接触浓度最高不超过200µg /mL;如果CD86的阳性值在1ug/mL,则对0.1ug/mL进行评估,以确认不会导致CD86超过阳性阈值的受试物的浓度;DMSO最终接触浓度不得超过0.4%。
选择标准:至少2个浓度与前一次试验相同;确认非细胞毒性下的最高CD86阴性浓度;确认所有非细胞毒性CD86阳性浓度;确认最低细胞毒性浓度;在EC150(或最高阴性非细胞毒性浓度)和CV70(或溶解度评估允许的最高浓度)之间均匀选择其他所需浓度;若前两次运行有差异,尽可能选择多的共同浓度;若存在干扰,需重新选择阳性浓度。
6.3 对照物处理
培养基对照、溶剂对照(与受试物同法稀释)、阳性对照松香酸(DMSO溶解,最终浓度50µg/ml)、阴性对照LA(完全培养基溶解,最终浓度200µg/mL),每种对照需要准备三对复孔。
6.4 细胞铺板及染毒
以3 x105个/ml细胞传代培养2天或以1.5 x105个/ml传代培养3天后,调整细胞浓度为5×105个/ml,取100µL/孔受试物工作液和100µL/孔细胞悬液1:1混合接种于96孔无菌平板中,每种条件下一对复孔,一孔用于CD86染色,一孔用于IgG1同型对照染色。每次CD86表达检测均需设置培养基对照、溶剂对照、阳性对照、阴性对照各三对复孔(当使用培养基作为溶剂时,溶剂对照与培养基相同),用密封带盖住板,在37±2°C,5±1%CO2,≥95%湿度下培养孵育45±3小时。
6.5 CD86表达检测
孵育结束后,检查并确定溶解度(若在显微镜下观察到晶体或液滴,则会产生干扰)。
用排枪将细胞吹两下从96孔平板对应移至V型板中,离心弃上清;
用100µL冰冷染色缓冲液清洗一次,然后在100µL染色缓冲液中重悬细胞;
用7-AAD染色细胞(5µL/孔,10min室温,避光);
用100µL冰冷染色缓冲液清洗一次,然后在100µL染色缓冲液中重新悬浮细胞;
用FITC标记的抗CD86或小鼠IgG1(5µL/孔,30min,4°C,避光)染色细胞;
用100µL冰冷染色缓冲液清洗两次;
用100µL冰冷PBS清洗一次;
在冰冷PBS中再悬浮细胞(96孔板中100µL或流式管中200µL)。
注意:整个染色操作应在冰上进行,在每一个洗涤步骤中,不要通过反复的移液来重悬细胞,而是在弃去上清液后通过短暂的涡旋来分散细胞即可。
用流式细胞仪对每组细胞的细胞存活率及CD86阳性细胞百分比进行测定。 分别以下用公式计算出受试物的细胞存活率(CV70)和受试物的细胞刺激指数(S.I.)。
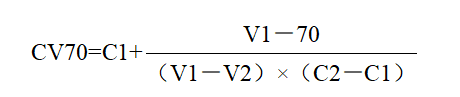
V1:大于70%最小细胞活性值
V2:小于70%最大细胞活性值
C1(μg/mL):V1对应的受试物浓度
C2(μg/mL):V2对应的受试物浓度

CD86+%:CD86阳性细胞百分比
6.6 流式细胞仪检测
绘制SSC/FSC散点图,调节仪器电压,圈出U937细胞群P1门;绘制7-AAD直方图,圈出活细胞P2门;绘制FITC/SSC散点图,放置十字门,分析细胞表面标记物CD86的表达。通过获取完全培养基/ IgG1孔表达值,设置FITC/SSC十字门分析标记,以便在可能的情况下,所有三个或至少两个完全培养基对照的IgG1位于 0.6至0.9%区域内;如果这无法实现,则设置分析标记,使一个完全培养基对照的IgG1在0.6至0.9%,另一个完全培养基对照的IgG1在0.9%至1.5%;如果这仍然无法实现,则IgG1数据分布太广,必须放弃运行。之后在不移动分析标记的情况下,测量每个孔中IgG1阳性细胞或CD86阳性细胞的百分比。
细胞显示在大小(FSC)和粒度(SSC)的散点图中,设置为对数比例(Log),以便清楚地识别第一门R1门中的(population)细胞群和消除碎片。
设置流式细胞仪,每孔获得P1门细胞10000个或包括死亡细胞在内的多达20,000个细胞,或在分析开始后一分钟内获取数据。
7 结果评价
7.1 试验成立条件
7.1.1 完全培养基对照细胞平均存活率> 90%;至少两个完全培养基对照的IgG1≥ 0.6且< 1.5%;若丢弃一个完全培养基对照的离群值后,剩下的两个完全培养基对照的校正后的CD86表达值应高于或低于其平均值的25%;完全培养基对照校正后的CD86基础表达值≥ 2%且≤ 25%。
7.1.2 DMSO溶剂对照的平均存活率> 90%;若丢弃一个DMSO对照的异常值后,剩下的两个DMSO对照的校正后的CD86表达值应高于或低于其平均值的25%;丢弃异常值后,DMSO溶剂对照CD86 S.I.的平均值小于250%。
7.1.3 阳性对照三对复孔中至少两个为阳性(CD86 S.I.≥ 150),必要时配制阳性对照系列浓度,应存在剂量反应。
7.1.4 阴性对照三对复孔中至少有两个为阴性(CD86 S.I. < 150%),且细胞活性≥ 70%。
7.2 致敏性结果判定
每种受试物至少进行两次独立的CD86表达检测试验。每种受试物表达检测试验,如果CD86 S.I.仅在最高非细胞毒性浓度下高于150%,则在第一次试验中无法判定。每次表达检测试验,如果CD86 S.I.在所有非细胞毒性浓度下低于150%,且无干扰(溶解度、颜色、细胞毒性),则该次CD86表达判定为阴性;如果CD86 S.I.高于150%,不论有无剂量反应和/或干扰,则该次CD86表达均判定为阳性。 如果两次试验CD86表达结果一致,则可判定该受试物是否具有致敏性;如果两次试验CD86表达不具有一致性,则需进行第三次试验。如果第一次试验无法判定,第二次与第三次结果不一致,则需进行第四次试验。最终的预测将基于三次或四次单独运行的结果来综合判定。
7.3 有效作用浓度计算
对于判定具有致敏性的物质,进一步计算其有效作用浓度值(Effective Concentration,EC),选用以下公式计算CD86的有效作用浓度值(EC150)。

S.I.1: S.I.< 150(EC150)最低刺激指数值
S.I.2: S.I.≥ 150(EC150)最低刺激指数值
C1(μg/mL): S.I.1对应的受试物浓度
C2(μg/mL): S.I.2对应的受试物浓度
8 结果解释
本试验结果能预测受试物的致敏性,但需应用合适的整合测试和评估方法(IATA)进一步评价受试物的致敏性,这些结果在有限的范围内外推到人类。
体外皮肤变态反应 U937细胞系激活试验
起草说明
为加强化妆品的监督管理,进一步提高化妆品使用安全性,中国食品药品检定研究院组织开展了体外皮肤变态反应 U937细胞系激活试验方法的起草工作。现就起草工作有关情况说明如下:
一、起草原则
试验要求和规定逐步与国际接轨,对于已经比较成熟的、被多数国家和组织认可的方法,原则上予以接受。对某些内容进行具体化和明确化,在尽量提高可操作性的同时,兼顾了技术发展的前瞻性。本方法制定过程中还注意了科学性和合理性、协调性和有效性,以及通俗性和规范性之间的关系。
二、起草过程
本研究由化妆品标准专家委员会于2018年立项,课题组在研究和分析国内外相关研究的基础上,对9种推荐物质进行了方法验证,并委托三家实验室进行实验室间验证,根据实验室验证过程和结果起草了试验方法文本。
三、与我国已有相关标准的关系
《化妆品安全技术规范》中用于检测皮肤变态反应的方法包括:皮肤变态反应试验、皮肤变态反应:局部淋巴结试验:DA(LLNA:DA)、皮肤变态反应:局部淋巴结试验:BrdU-ELISA(LLNA: BrdU-ELISA)、化妆品用化学原料体外皮肤变态反应:直接多肽反应试验(DPRA)。其中皮肤变态反应试验、LLNA:DA、LLNA: BrdU-ELISA均使用动物(豚鼠、小鼠)进行试验;DPRA方法针对皮肤变态反应AOP中的第一个关键分子事件进行检测。U937细胞系激活试验(U-SENSTM)针对皮肤变态反应AOP中的第三个关键分子事件进行检测。未来该方法可以应用在皮肤致敏评价的整合策略中,进一步提高替代试验方法的准确性和特异性。
本研究建立了皮肤变态反应的替代试验方法,以期与国际标准接轨,与《化妆品安全技术规范》中皮肤变态反应检测方法在技术上形成互补,建立我国动物实验替代方法体系,增补、修订和完善现有的标准与规范方法以及促进我国未来的化妆品安全评价体系提供技术支持。
四、与国际同类标准的关系
2016年该方法通过欧盟替代方法验证中心科学咨询委员会(ESAC)独立同行评议,2018年,经济合作和发展组织(OECD)正式发布U-SENS™方法的操作指南(OECD-442E),将其用于化学物质皮肤致敏性的安全评价。
本方法涵盖了OECD 2018年正式发布的“皮肤致敏反应有害结局通路中关于树突状细胞活化的关键事件的体外试验方法操作指南:U937细胞系激活试验”(OECD GUIDELINE FOR THE TESTING OF CHEMICALS In Vitro Skin Sensitisation assays addressing the Key Event on activation of dendritic cells on the Adverse Outcome Pathway for Skin Sensitisation ANNEXⅡ: U937 CELL LINE ACTIVATION TEST (U-SENS™))的要求,基本操作和OECD U-SENS™方法一致,具体变动内容包括:
(1)OECD方法中的阳性对照为“2,4,6-三硝基苯磺酸”属于危险化学品,因此,在本试验中增加阳性对照物质“松香酸”。
(2)在标准中对操作方法进行细化,如“铺板过程混匀防止细胞沉降”“轻轻涡旋清洗细胞”,以提高方法的可操作性。
各项技术内容的依据来源自OECD GUIDELINE FOR THE TESTING OF CHEMICALS In Vitro Skin Sensitisation assays addressing the Key Event on activation of dendritic cells on the Adverse Outcome Pathway for Skin Sensitisation ANNEXⅡ: U937 CELL LINE ACTIVATION TEST (U-SENS™)(OECD 《化学品测试指南》TG 442E,2018年),基本涵盖了其对采用对象、实验操作和结果分析的技术要求,并通过试验确认。
五、实验室验证结果
本方法实验室内验证结果和OECD参考值范围均一致;委托3家单位对方法进行实验室间验证。所有单位对8种化学物的定性预测结果均一致;4家实验室对8种OECD参考物质的定量检测结果(CV70、EC150)与OECD TG 442E附表中规定范围相比,准确率均为为100%。


