化妆品原料《急性吸入毒性试验 急性毒性分级法》的评价(征求意见稿)
急性吸入毒性试验 急性毒性分级法
Acute Inhalation Toxicity Acute Toxic Class Method
(征求意见稿)
1 范围
本试验方法规定了急性吸入毒性试验 急性毒性分级法的试验原则、试验方法、数据和报告。
本试验方法适用于化妆品原料急性吸入毒性的急性毒性分级。
2 试验目的
本试验方法的目的是通过测试获得受试物的健康危害信息等资料,从而可参考联合国全球化学品分级和标签管理协调制度(the United Nations(UN)Globally Harmonized System (GHS)of Classification and Labelling of Chemicals)的化学品急性吸入毒性分级标准对其急性毒性进行分级。本试验方法适用于单一成分的化妆品原料,非单一成分的原料若使用本方法进行评价,需要提供更多的科学依据说明其可行性。本试验方法不适用于测试难溶的同分异构物、纤维类、纳米类原料等。
3 定义
急性吸入毒性分级法是指按照一定的连续试验步骤和相应的浓度进行测试,从而获得受试物的毒性分级和半数致死浓度(LC50,Lethal Concentration 50)估测范围的试验方法。
理论浓度(nominal concentration),是指应用受试物的量除以通过染毒系统空气的总体积所得到的浓度。
实际浓度(actual concentration)是指在吸入式染毒柜中动物呼吸道中的受试物浓度,可通过特异性(如直接采样、吸附或化学反应等方法进行采样、分析)或非特异性(如滤膜增重法)等方法进行测试分析。
4 试验原则
本试验采用分步试验的方法,观察试验动物段时间(一般为4 h,不超过24 h)吸入暴露后的反应,从而得到可以对受试物急性吸入毒性进行分级的信息。每步试验使用每种性别3只动物在确定的浓度下进行吸入暴露试验。根据动物死亡和/或濒死状态,有时只进行2步试验操作就可以对受试物的急性吸入毒性类别做出判断。如果有证据表明某种性别的动物比另外一种动物的敏感性要高时,可以只使用敏感性别动物进行试验。前面一步操作的试验结果决定着下一步试验操作:
a)无需进行下一步试验;
b)每种性别3只动物;或
c)只使用6只敏感性别的动物。方法是每个试验浓度组使用6只敏感性别的动物(性别不限),以估测的毒性类别界限范围数值中较低的浓度来进行试验。
应人道地处死濒临死亡的、处于难以忍受疼痛的和严重持久痛苦的动物按照试验死亡进行统计。
5 试验方法
5.1方法描述
5.1.1 动物种属的选择
应使用健康年轻、实验室中常用的种属动物进行试验。首选大鼠,如使用其他动物应进行论证,说明理由和依据。
5.1.2 动物的准备
雌性动物应是未经产的、未妊娠。要保证每步试验暴露时的鼠龄在8周~12周;每一步试验之间使用的同周龄、同性别动物的平均体重相差应不超过±20%。采用随机选择原则,并对每只动物做出标记。在进行试验之前至少要在笼内饲养5天以适应实验室饲养条件。试验前还需在试验设备中进行短期的适应训练,以减少因为进入新的设备环境造成的应激。
5.1.3 饲养条件
实验动物暴露前和暴露结束后,室内温度应在22℃±3℃。理想情况下相对湿度在30%~70%范围内,但试验暴露期间以水为载体时很难做到。
实验动物暴露前后按性别、浓度分笼饲养,但是每笼动物的数量不能妨碍对每只实验动物的观察,并应减少由于同种相残和相互撕咬而造成实验动物信息的丢失。以口-鼻式装置暴露时,需将动物放入染毒柜内使其适应染毒柜的环境。动物在染毒柜内的固定不能过度的增加动物体力、热量和活动的负荷,动物的固定可能影响动物的体温(过热)和/或每分钟动物呼吸量。如果有资料表明这些改变没有达到可感觉到的程度,就不一定需要预先在染毒柜内进行适应操作。全身暴露气溶胶的动物暴露期间需各自相隔互不接触,防止柜体内动物的相互趴卧造成被毛对气溶胶的过滤作用。除暴露期间外,可使用常规和经过认证的实验室饮食,自由饮水。采用人工照明,每12 h明暗交替。
5.1.4 吸入染毒装置
要根据受试物的性质和试验目的来选择吸入染毒方式。首选的染毒方式是口-鼻式染毒(包括头部暴露、鼻部暴露或者口鼻部暴露模式)。当受试物是液体、固态气溶胶和能产生气溶胶的蒸气时,首选鼻式暴露方式。对于特殊的研究目的,也可采用全身暴露染毒装置以更好地满足研究需求,但应在试验报告中予以阐释说明。为了保证全身染毒时柜体内空气中受试物的稳定性,实验动物的总体积不应超过染毒柜总容积的5%。
5.2 暴露条件
5.2.1染毒浓度
5.2.1.1推荐暴露吸入时间为4 h,但需除去达到浓度稳定平衡所需时间。根据特殊试验需要也可采用其他的暴露时限,但是需在试验报告中给予相关说明。全身暴露时的动物单独饲养,防止染毒柜内其他动物的理毛行为经口摄入受试物。吸入暴露期间需要禁食。全身暴露时可提供饮水。
5.2.1.2动物吸入暴露的受试物是气体、蒸气、气溶胶或是它们的混合物。试验时将受试物制备成的何种物态(气溶胶、粉尘)取决于受试物的理化性质、设定的浓度,和/或按照实际加工使用期间的物理状态等。具有吸湿性的和会发生化学反应的受试物在试验中需保证吸入的空气是干燥的。需注意避免使用发生爆炸的浓度进行试验。
5.2.2 颗粒粒径的分布
对所有的气溶胶和可能形成气溶胶的蒸气都需测定颗粒粒径的大小。为了使整个呼吸道都能暴露受试物,推荐的气溶胶颗粒的质量中值空气动力学直径(Mass Median Aerodynamic Diameter,MMAD)为1μm~4μm,其几何标准差为1.5~3.0。需尽可能达到此标准,如技术上无法满足要求时需由专家做出评判。例如,金属烟尘比本标准的粒径要小,但是带电的粒子、纤维和吸湿性受试物(在呼吸道潮湿环境下其粒径增加)可超过这个标准。
5.2.3 载体选择与受试物的配制
为了制备具有合适浓度和粒径大小的受试气体,需要使用载体溶剂,水是首选载体溶剂。颗粒物需要机械加工达到要求的粒径大小,但要注意加工中是否引起受试物的分解和变性。如机械加工改变了受试物组成成分(由于过度摩擦产生高温),受试物的组成要经过检测分析进行确认。需注意不要污染受试物。对于不能形成可吸入性的或不易形成粉末的颗粒材料不需要进行试验。磨损试验是用来证明加工这些材料时不会产生呼吸性颗粒物。如果经磨损试验证实可产生呼吸性颗粒物,该被加工的材料应当进行吸入毒性试验。
5.2.4对照组
当使用的受试物载体及阴性(仅吸入气体)的有历史背景数据时,一般不需要平行设置载体对照组或阴性(仅吸入气体)对照组。
5.3 暴露条件的监测
5.3.1 染毒装置内气流
通过染毒柜的气流速率需严格控制,可连续在线监测记录或每次暴露期间至少每小时监测记录一次。试验所用空气中受试物浓度(或其稳定性)的监测数据是对染毒系统中各个动力学参数作用的综合结果,因此这些数据可提供控制制备动态空气设备相关参数的间接方法。在口-鼻式染毒时,当通过染毒系统的试验气体的气流动力不足时,需注意动物的在染毒装置内是否发生重复吸入。已有确定在所选定的操作条件下不会发生重复吸入的方法。氧气的浓度至少为19%;二氧化碳的浓度不超过1%。如果证实确实不能达到这个标准,需要测定并记录试验气体中氧气和二氧化碳的浓度。
5.3.2染毒装置柜体内温度和相对湿度
染毒柜内温度维持在22℃±3℃。口-鼻式和全身暴露都需监测记录动物呼吸带的相对湿度,在吸入染毒的4 h之内至少3次;吸入染毒暴露期限较短的试验可以每小时监测记录1次。理想的相对湿度需维持在30%~70%;但是有时很难达到(例如:受试物的水制备物),有时是受试物与测定方法发生干扰而无法测定。
5.3.3 受试物
5.3.3.1 理论浓度
无论何时都应尽量记录并计算染毒柜空气中的理论浓度。理论浓度是指制备产生的受试物的量除以通过染毒系统的空气总体积得到的参数。虽然理论浓度不是用来描述动物暴露特征,但是通过理论浓度与实际浓度进行比较可以得到试验系统制备效率的指征,从而可发现制备染毒空气过程中存在的问题。
5.3.3.2 实际浓度
1) 实际浓度是吸入染毒柜内动物呼吸道中的受试物的浓度,可以通过特异性的方法(如吸附或化学反应)直接采样,然后进行分析;或是通过非特异性的方法(如滤膜增重法)来获得。单一成分的粉末、低挥发性液体的气溶胶才能使用增重法,同时还需要专门预试验数据的支持。对多成分的粉末气溶胶也可以用增重分析法测量,但是这需要证实所制备的空气与最初受试物的组成成分相似。如果没有此类数据资料,则需在试验期间按照规定的时间间隔对制备产生的空气进行再分析(理想的是染毒柜中的空气)。对可挥发的或易升华的气溶胶,需证实所用方法能收集到所有物体状态的受试物。需在试验报告中报告靶浓度(目标浓度)、理论浓度和实际浓度,但只有实际浓度可用来计算致死浓度值。
2) 尽量使用同一批试验受试物。应将试验样本保存在能维持纯度、均匀性和稳定性的条件下。开始试验前对受试物的特征有充分的了解和描述,如纯度、鉴别特征和鉴定出来的污染物和杂质。这可用以下参数来证实,如保留时间、相对峰面积和通过质谱、气相色谱或其他的检测方法得到的分子量,包括且不限于以上内容。检验检测机构需要对委托方提供的受试物进行必要的简单描述(如颜色、物理状态等)。
3) 需尽可能的保持染毒空气成分稳定,可采用适当的分析方法连续或间隔采样监测。间隔采样时,吸入染毒4 h的试验至少采样2次。如果由于系统内染毒空气流量过低所限,或染毒浓度太低需采集较多的空气样本时而不能完全满足连续或间隔采样量的要求,可在整个暴露期内只采集一次样本。如果样本之间出现明显波动,进行下一个浓度试验时需在暴露期间采集4次样本进行分析。空气各个样本之间的浓度波动范围规定,气体和挥发性受试物不得超过平均浓度±10%,液体或固体气溶胶不超过平均值的±20%。并需要计算柜内空气受试物达到95%平衡时的时间(T95)。一个暴露周期内需要考虑到制备受试物空气的时间和达到T95的时间。对组成非常复杂混合物的蒸气/气体、气溶胶(如推动终端装置设备产生的燃烧空气和试验物形成的)在染毒柜内空气中每一相成分物相各不相同,至少要选择一个标志性物质来进行分析,通常是受试制备物中处在某一物相(蒸气/气体或气溶胶)的主要的活性物质。如果试验物质是制剂(商品形式的产品)分析报告的浓度应是制剂的总浓度,不是活性成分的或某成分的浓度。
5.3.3.3 颗粒物粒径的分布
气溶胶的粒径大小需在染毒的4 h期间至少测定2次,方法是使用撞击采样器或其他替代的设备如空气动力学粒径仪等。如果撞击时采样器与替代的测定方法所得到的结果相同,在整个试验期间的就可以使用替代的方法进行监测。后一种检测方法,如滤膜增重或尘埃测定器/气体发泡收集管等,与最初确定的测定方法进行平行试验,来验证原来测定方法的收集效率。粒径大小分析得到的质量浓度应与采用滤膜分析法得到的质量浓度的一个合理的限度之内。如果在试验开始阶段就证明两种试验方法的质量浓度相同,就可以免去验证性试验。从动物福利方面考虑,需采取措施减少无确定结果的数据资料,因为这会要求重复进行暴露试验。如果空气中的蒸气受试物能发生凝结而形成气溶胶,或者染毒蒸气空气中测定到颗粒物也就是暴露空气存在潜在的混合相,需对这种受试物进行粒径的测定。
5.4 操作步骤
5.4.1正式试验(main test)
5.4.1.1 每一步使用雌雄各3只动物,或6只敏感性别的动物。如果采用鼻式暴露时使用的啮齿类动物不是大鼠,需要调整最长的暴露时间以减少动物种属之间的差异。可从4个固定的起始浓度水平染毒,这个浓度应能引起染毒动物中的某些动物出现毒性作用。气体、蒸气和气溶胶的试验步骤图(见7试验步骤流程图)的浓度水平是第1类~4类的分级标准的界限值:气体为(100、500、2500、20000 ppm/4 h)(见图1);蒸气为(0.5、2、10、20 mg/L/4 h)(见图2);气溶胶为(0.05、0.5、1、5 mg/L/4 h)(见图3)。高于各相应物态类别的上限浓度就归为第5类。按照各自的试验图表来确定起始浓度。根据人道处死和动物死亡的数量,按照图中的指示的箭头来决定下一步的试验,直到能对受试物作出毒性分级时结束试验。
5.4.1.2 进行下一个暴露浓度组试验的时间间隔长短要根据毒性体征的发作时间、持续时间和严重程度来决定。决定进行暴露下一个浓度水平需要直到前一个浓度水平的动物存活状态完全确定下来后再进行。建议的每个浓度水平之间的时间间隔为3至4天,这可以观察到可能存在的迟发毒性。如出现的反应不能确定,可适当调整时间间隔的长短。
5.4.2 限度试验(limit test)
5.4.2.1如已知或预期受试物几乎无毒时可进行限度试验,如在超过规定的极限浓度值以上时才引起毒性反应的受试物。受试物的毒性的信息可从已经检测的类似化合物、混合物或产物结果得到,此时要考虑到已知的具有毒理学意义的受试物的特性、混合物构成的百分比等。在没有或很少毒性信息的情况下,或者是估计受试物是具有毒性,需进行正式试验(可参考OECD指南39号)。
5.4.2.2 正常的操作程序下,使用每种性别3只动物,或使用6只敏感性别的动物,暴露水平分别是:气体20000 ppm;蒸气20 mg/L;粉尘/雾5 mg/L(如果技术可达到)。受试物制备成气溶胶时,粒径的大小需达到可呼吸性粒子的大小(如MMAD为1μm~4μm)。绝大部分的受试物都能在2 mg/L的浓度水平进行试验。如进行高于2 mg/L浓度水平的气溶胶试验,受试物应能够制备成可呼吸性粒子大小。从动物福利方面考虑,不主张超过限度浓度的试验。
5.4.2.3 只在有可能直接涉及到人类健康需要的情况下才进行第5类染毒浓度水平(>20000 ppm或mg/L)的试验,并需在试验报告中论述理由。对潜在爆炸性受试物试验设计时要认真研究避免引起发生爆炸的条件出现。为了避免不必要的使用动物,开始限度试验前,需在染毒系统不放置动物的条件下进行预试验,以确认染毒条件是否能达到限度试验的水平。
5.4.3 观察
5.4.3.1 暴露期间要对实验动物经常进行临床观察。暴露染毒结束后的当日至少要观察2次,还可根据动物对染毒的反应增加观察次数;此后的14天内至少每日观察1次。观察周期时长不是固定不变的,需要根据出现的临床症状的特点、时间以及恢复期的长短决定。毒性反应出现和消失的时间很重要,应特别注意是否存在毒性体征延迟的倾向,对每只动物的所有的观察都要分别作系统的记录。
5.4.3.2 对处于濒死的动物和表现出严重的疼痛和/或持续的严重痛苦的动物从动物福利考虑要人道的处死。对最初出现的微弱的毒性体征和由于暴露操作引起的短暂的呼吸道的异常改变等临床体征要认真分析区别,不要错误认为这些都是染毒处理引起的毒性作用。要按照列在人道观察终点的指南文件中“人道终点”的原则和标准进行操作。对人道处死的或发现已经死亡的动物处死和死亡时间要尽可能的准确的记录。笼外观察包括动物皮肤和被毛、眼和粘膜、呼吸、循环、自主神经和中枢神经系统的改变,以及身体活动和行为方式等变化。尽可能的注意局部作用与系统作用之间的任何差别。关注点主要为颤动、抽搐、流涎、腹泻、嗜睡、睡眠和昏迷。测定直肠温度可辨别出是否存在因染毒或在染毒柜内过度的限制造成的反射性呼吸过缓、体温过低/过高。
5.4.4 体重
进入实验室适应环境期间每只至少要称重一次;染毒当日开始试验前(第0天)、染毒后的1、3、7天(此后每周记录一次)、染毒第1天后死亡或进行人道处死的动物进行称重。体重变化是判定毒性作用的指标,并且对于体重持续低于染毒前体重的20%要给予密切观察。试验结束时存活动物称量体重后并人道地处死。
5.4.5 病理学
所有实验动物,包括试验期间死亡的、人道处死的动物和动物福利考虑从试验队列中退出的,都需进行大体解剖检查。如果发现动物死亡后不能立即进行解剖检查,将死亡动物放入冰箱的冷藏箱内低温存放,以减少动物尸体的自溶分解。大体尸检应在死亡后1 d~2 d进行。每只动物大体解剖所见的病理学改变都记录,特别注意呼吸道出现的任何变化。其他辅助的检查,包括可能对试验结果做出解释的检查指标,如测定存活大鼠的肺脏重量或者对呼吸道进行显微检查以提供受试物刺激性的证据等。检查的器官涉及到染毒后存活24 h以上的动物出现大体解剖学改变的器官、或者已知或预期可能受到影响的器官。全呼吸道的显微组织学检查为鉴定受试物是否与水发生反应(如,酸和吸湿性的受试物反应)提供非常有价值的信息。
6 数据和试验报告
6.1 数据
需提供每只动物的体重、大体解剖检查所见的全部资料。临床观察的数据需要总结成表格的形式以体现出每个试验组使用的动物数、出现特异性毒性体征的动物数、试验期间死亡或人道处死的动物数、每只动物的死亡时间、详细描述毒性作用的发生、发展的时间进程和体征的可逆性;大体解剖所见。
6.2 试验报告
试验报告需包括以下信息:
1)实验动物和饲养条件:
— 饲养笼具的描述:每笼动物的数量(或动物变化的数量)、垫料、环境温度、相对湿度、光照周期、饲料合格认证资料;
— 使用的动物种属和品系,不使用大鼠进行试验的论证依据;
— 动物的数量、周龄和性别;
— 随机选择分组的方法;
— 动物食物、饮水的质量(包括饲料的类型/来源和供水的来源);
— 试验前的所有的包括饲料、检疫、疾病的处理等描述。
2)受试物:
— 物理性状、纯度、相关的理化性质(包括同分异构体);
— 受试物特征性数据和化学文摘(CAS)注册号(如果已知)。
3)载体:
— 如果不是用水作为载体,所用的载体是什么,对采用这种载体的理由作出论述;
— 载体的历史背景数据或所使用的载体不会干扰试验结果的数据资料。
4)吸入染毒装置:
— 吸入染毒装置的介绍,包括大小尺度和体积;
— 除了描述制备染毒空气操作外,还需动物暴露所用设备及其来源进行描述;
— 测定气温、湿度、粒径大小和实际浓度的仪器设备;
— 空气的来源、空气供给/解压处理、调节供给条件所使用的系统;
— 确保试验空气均匀所使用的调节设备和方法;
— 压差(正压或负压);
— 每个吸入装置动物暴露孔的数量(口-鼻式装置);每个染毒装置的动物数(全身染毒设备);
— 试验时空气中受试物的均匀性、稳定性;
— 温度和湿度感受器、采样孔所在的部位;
— 空气流速,包括口-鼻式固定孔处的空气流速、全身染毒柜内放置动物处的空气流速;
— 如果测定了空气中氧气和二氧化碳需要提供所用设备的信息;
— 达到吸入染毒柜空气浓度稳定平衡的时间(T95);
— 每小时空气体积更换次数;
— 计量仪器设备。
5)暴露数据:
— 正式试验中选择设定靶浓度的理由(基本原理);
— 理论浓度(制备的试验物质进入到吸入染毒设备的总量除以通过染毒柜空气的总体积);
— 从动物呼吸道中采样测得的受试物的实际浓度;对于不同物态的混合物受试物(气体、蒸气和气溶胶),需分别对每一物态进行测定;
— 报告中所有的空气浓度都用质量单位(如mg/L,mg/m3等)或体积单位(如ppm、ppb)来表示;
— 颗粒物粒径大小的分布用MMAD和GSD来表示,同时列出得到此参数数值的计算过程。应在报告中记录每个检测到的粒径大小的数据。
6)试验条件:
— 受试物制备的详细操作,包括固态物质被制备成为直径更小的颗粒物或制备成溶液的详细操作过程;如机械加工时改变了受试物的组成成分,还要提交加工后受试物组成成分的检测分析的结果;
— 制备试验空气所用设备和制备动物染毒时所用空气的操作的描述(可以用示意图表示);
— 所用化学分析方法的详细描述和分析方法可靠性的详细描述(包括空气媒介样本中受试物的回收率);
—设置染毒浓度的基本原理。
7)结果:
— 列表表示染毒装置内空气环境的温度、湿度和流速;
— 列表表示染毒空气中理论浓度、实际浓度数据;
— 列表表示颗粒粒径大小的数据,包括样本的采集测试方法、粒径大小的分布、MMAD及GSD的计算等;
— 列表表示动物出现毒性反应的数据和每只动物暴露浓度水平(如死亡率、性质、严重程度和作用的持续时间等毒性体征的动物数量);
— 试验中测得的每只动物的体重、计划试验结束人道处死前动物死亡的日期和时间、毒性体征出现的时间和过程,以及每只动物出现的毒性体征是否是可逆的等;
— 每只动物大体解剖和组织病理学检查(如果进行了组织学检查)所见;
— 受试物按照急性吸入毒性分级属于哪类和LC50界限值。
8)讨论和结果分析:
— 需要特别强调的是需要描述是否达到本标准规定的参考值范围,如限度浓度试验和颗粒粒径大小的规定;
— 应根据总体调查结果处理颗粒的可吸入性,尤其是当无法满足颗粒尺寸标准时;
— 对测定理论浓度和实际浓度所采用的方法的一致性进行评价;并对整个试验过程中都要涉及到的理论浓度与实际浓度的相互关系进行评价;
— 对动物可能的死亡原因和主要的作用机制(是系统毒性或局部毒性)作出分析估测;
— 如果因为动物疼痛、或表现出严重的持久的痛苦状态而被人道处死,要根据OECD人道终点标准的指导文件作出解释说明。
7 实验步骤流程图
图1:各初始气体浓度应遵循的试验程序(ppm/4 h)
对于每一种起始气体浓度,本图中所列的相应检测方案概述了应遵循的试验程序。根据实施人道处死或死亡动物的数量,试验程序遵循箭头指示。
图1a:起始浓度为100 ppm
图1b:起始浓度为500 ppm
图1c:起始浓度为2500 ppm
图1d:起始浓度为20000 ppm
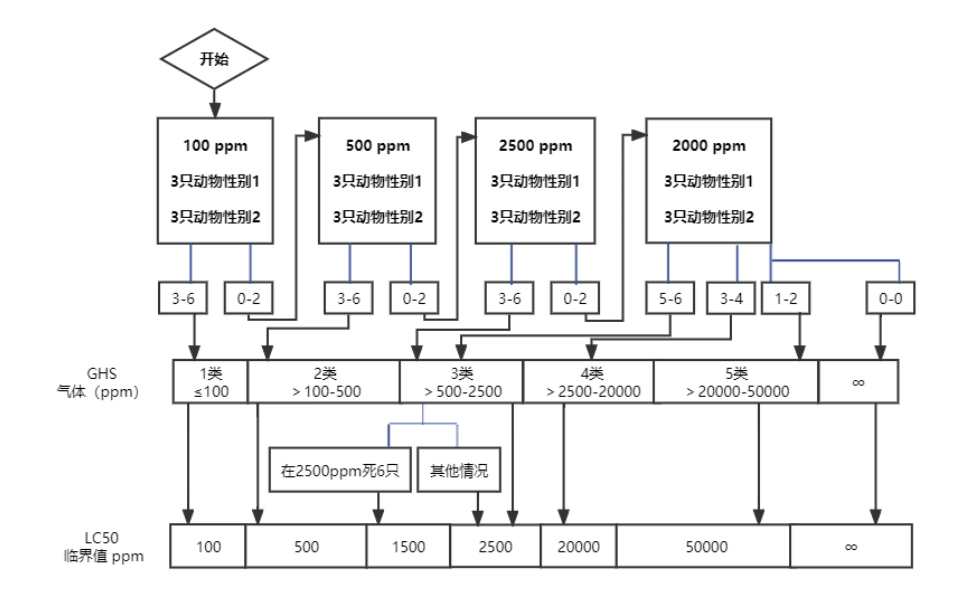
图1a:气体的起始浓度为100 ppm/4 h的试验程序

图1b:气体的起始浓度为500 ppm/4 h的试验程序

图1c:气体的起始浓度为2500 ppm/4 h的试验程序

图1d:气体的起始浓度为20000 ppm/4 h的试验程序
图2:蒸气的各起始浓度应遵循的程序(mg/L/4 h)
对于每一个起始气体浓度,本图中所列的相应检测方案概述了应遵循的试验程序。根据实施人道处死或死亡动物的数量,试验程序遵循箭头指示。
图2a:起始浓度为0.5 mg/L
图2b:起始浓度为2.0 mg/L
图2c:起始浓度为10 mg/L
图2d:起始浓度为20 mg/L

图2a:蒸汽的起始浓度为0.5 mg/L/4 h的试验程序

图2b:蒸汽的起始浓度为2 mg/L/4 h的试验程序

图2c:蒸汽的起始浓度为10 mg/L/4 h的试验程序

图2d:蒸汽的起始浓度为20 mg/L/4 h的试验程序
图3:粉尘和雾的各起始浓度应遵循的程序(mg/L/4 h)
对于每一个起始气体浓度,本图中所列的相应检测方案概述了应遵循的试验程序。根据实施人道处死或死亡动物的数量,试验程序遵循箭头指示。
图3a:起始浓度为0.05 mg/L
图3b:起始浓度为0.5 mg/L
图3c:起始浓度为1 mg /L
图3d:起始浓度为5 mg /L

图3a:粉尘和雾的起始浓度为0.05 mg/L/4 h的试验程序

图3b:粉尘和雾的起始浓度为0.5 mg/L/4 h的试验程序

图3c:粉尘和雾的起始浓度为1 mg/L/4 h的试验程序

图3d:粉尘和雾的起始浓度为5 mg/L/4 h的试验程序
急性吸入毒性试验 急性毒性分级法
起草说明
为配合《化妆品新原料注册备案资料管理规定》的实施,有必要建立与其相适应的化妆品原料急性吸入毒性试验-急性毒性分级的试验方法,从而为化妆品原料的安全性评估提供技术保障,中国食品药品检定研究院组织起草了《急性吸入毒性试验 急性毒性分级法》(征求意见稿)。现就起草的有关情况说明如下:
一、起草的必要性
随着我国在2021年2月发布《化妆品新原料注册备案资料管理规定》,针对化妆品新原料,要求提供相应的毒理学安全性评价资料、安全风险评估资料等内容。化妆品原料种类众多,接触或进入人体的方式多种多样,有经皮、经口、经过粘膜、经过呼吸道等多种方式,产生的潜在安全影响均需要全面评价,以确保化妆品原料在注册、备案的过程中的安全性得到充分的关注,从而为化妆品的安全应用奠定坚实的技术基础。
通过喷洒等方式使用的化妆品原料及产品,如具有香氛、除臭等功能的原料或产品,常常可通过吸入的方式进入体内,因此,尽快完善相应原料的安全评价技术方法,具有重要的现实意义。
国际经济合作与发展组织(Organization for Economic Co-operation and Development,OECD)基于科学技术的发展、管理规定及动物福利等方面的考虑,于1981年公布实施了急性吸入毒性测试导则(OECD 403),由于在2001年公布实施了急性经口毒性分级法(TG 423)后,才考虑编制相应的急性吸入毒性分级法(Acute toxic class, ATC)。对急性吸入毒性分级法(ATC)数据质量的回顾性评估表明该方法非常适合与对化学物的毒性分级和产品标签规定的需要。2009年9月OECD公布实施了化学品测试导则NO.436(2009)《急性吸入毒性试验:急性毒性分级法》,对急性吸入毒性的试验原则、方法、数据和试验报告、附录等内容进行了规定。2012年7月,中华人民共和国国家质量监督检验检疫总局、中国国家标准化管理委员会发布了中华人民共和国国家标准《化学品 急性吸入毒性试验 急性毒性分级法》GB/T 28648-2012,对化学品急性吸入毒性试验急性毒性分级法的适用范围,原则、方法、数据、报告等内容进行了规定,其中核心的主要内容是针对化学品的急性吸入毒性进行分级。
2021年,我国发布了《化妆品新原料注册备案资料管理规定》,对化妆品新原料注册备案资料要求进行了明确规定。因此,对化妆品原料的急性吸入毒性进行分级评价,对未来化妆品原料的安全状况、适用范围、使用形式等都具有重要的参考意义,值得尽快将该类技术评价方法予以完善。
二、起草原则与思路
查阅国内外关于化学品急性吸收毒性的试验方法,重点针对OECD化学品测试导则NO.436(2009)《急性吸入毒性试验:急性毒性分级法》、中华人民共和国国家标准《化学品 急性吸入毒性试验 急性毒性分级法》GB/T 28648-2012中规定的相关内容,对相应的试验方法进行比对、分析,进而转化,建立适用于化妆品原料安全性评价的急性吸入毒性试验 急性毒性分级法。在建立急性毒性吸入毒性试验 急性毒性分级试验方法时,明确了该方法适应于化妆品原料评价的适用范围,对试验目的、实验原则、实验方法中涉及的试验动物、吸入染毒装置、暴露监测、试验操作、试验观察、组织病理学结果、试验数据及报告等内容,进行了详细梳理和规定,起草了《急性吸入毒性试验 急性毒性分级法》(征求意见稿)。
三、主要内容
(一)适用范围
关于《急性吸入毒性试验 急性毒性分级法》适用范围的问题,通过对OECD化学品测试导则NO.436(2009)《急性吸入毒性试验:急性毒性分级法》、中华人民共和国国家标准《化学品 急性吸入毒性试验 急性毒性分级法》GB/T 28648-2012中相关内容的研究、分析,从试验方法的角度而言,该方法主要适用于原料急性毒性的分级,OECD和国标都是适用于“化学品”,也即是归属于化学品的原料。关于该方法在化妆品领域的适用性问题,也召开过专题讨论会,专家认为,从急性吸入毒性分级试验设置的目的来看,也只能是针对化妆品原料,只有原料才有必要对相应的急性吸入毒性进行分级,化妆品产品不存在急性吸入毒性分级的问题。因此,在该方法的适用范围方面,还是确定该方法适用于化妆品原料的急性吸入毒性分级评价,并且认为该方法适用于单一成分的原料,对非单一成分的原料,若应用该方法进行评价,需要提供更多的科学实验数据来证明其可行性。
(二)实验动物
根据国内外文献、动物伦理要求和试验指导原则对试验动物的种类、性别、周龄、体重、数量、饲养条件、适应性饲养时间等条件进行规定,并根据急性吸入毒性试验的特点对普通试验动物和敏感试验动物的性别和数量进行了特殊规定,即常规一般是每性别3只动物,或只使用敏感性别动物6只。
(三)吸入染毒途径的选择
根据试验方法对中受试物可能的吸入途径进行了规定,吸入途径包括仅头部暴露、鼻部暴露和鼻口部暴露三种吸入模式,一般首选口-鼻式染毒。
(四)暴露染毒的控制和监测
暴露条件是确保暴露染毒稳定可控的关键,涉及暴露染毒时间、受试物制备、受试物颗粒粒径分布、受试物载体配制的选择、对照动物的设置等多个方面,该方法都进行了相应的规定。
在满足暴露条件的前提下,如何对暴露情况进行监测,是确保后期染毒结果的核心,包括对染毒装置气流速率的严格控制,需连续在线监测记录或暴露期间至少每小时监测记录一次等,另外,还需要控制染毒装置的相对温度、湿度等,均是确保监测结果能符合要求的关键环节。
(五)试验操作要求
正式试验一般每步使用雌雄各3只动物,或6只敏感性别动物。根据不同的受试物状态,如气体、蒸汽或气溶胶,可根据附件中的试验步骤图,采用不同的起始浓度开展相应的试验。
(六)试验结果采集
染毒后对试验动物的观察和试验结果采集是确保试验结果科学、可靠的关键。因此,方法规定了暴露染毒后,试验观察的频率、周期、毒性体征的观察记录、动物人道主义处理的要求、试验动物的体重、组织病理学的要求等各项内容。
(七)试验报告
试验报告要求具体详实,包括实验动物、受试物、载体、吸入装置、暴露数据、试验条件、试验结果等各个方面的内容。
四、技术路线



