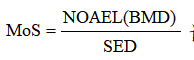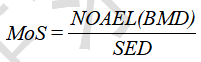当前位置:首页 > 搜索 "致敏性"
中检院关于发布《皮肤致敏性整合测试与评估策略应用技术指南》的通知
致敏性整合测试与评估策略应用技术指南》(见附件),现予发布。特此通知。附件:《皮肤致敏性整合测试与评估策略应用技术指南》中检院2024年7月8日附件1:《皮肤致敏性整合测试与评估策略应用技术指南》.doc......
中检院《皮肤致敏性整合测试与评估策略应用技术指南》问答
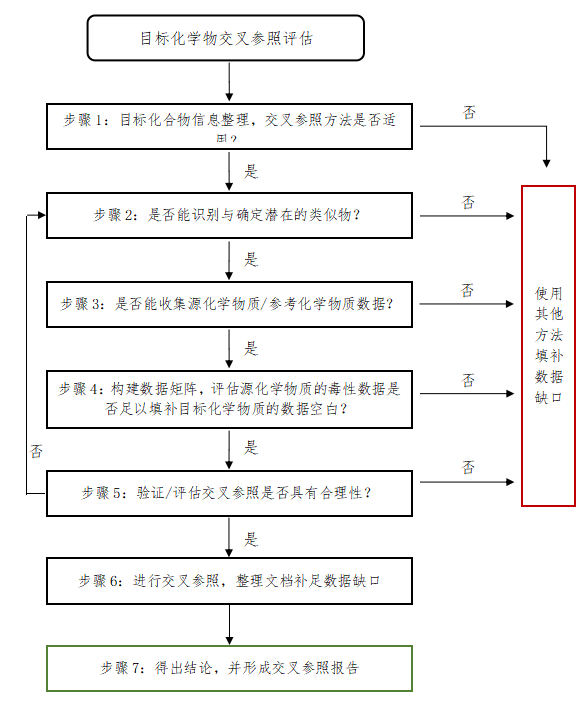
致敏性整合测试与评估策略是化妆品原料皮肤致敏性评价的工具之一,根据评估目的、整合的信息源、覆盖了哪些关键事件、评估程序、结果判定要求等因素的不同,可组成不同的“整合测试与评估策略”。基于我国化妆品行业现状,本次发布的为“3选2试验”策略,基...
李锦聪 - 《化妆品安评与毒理系列课程》 - 报名即学
致敏性光毒性光变态反应遗传毒性重复剂量毒性生殖发育毒性慢性毒性致癌性吸入暴露危害识别人群流行病学剂量反应关系评估阈值的毒性效应基准剂量NOAELBMD发生肿瘤的剂量有害作用的最低剂量LOAEL安全边际值暴露评估暴露部位暴露频率暴露量透皮吸收...
口腔清洁护理用品安全评估指南(GB/T 42763-2023)
致敏性资料,例如GPMT资料,或豚鼠局部封闭涂皮试验资料,或LLNA资料,或经权威机构(如OECD、国内外监管部门等)认可的体外替代试验资料等。5.2.4遗传毒性资料,至少包括一项基因突变试验和一项染色体畸变试验资料。5.2.5重复剂量.....
《化妆品安全评估资料提交指南》
致敏性的风险在可接受范围内。(三)特定类型化妆品原料的安全评估1.香精香料1.1产品配方表“标准中文名称”栏中仅填写“香精”原料的,应按照《导则》的原则和要求对香精进行评估,或明确产品所用香精符合国际日用香料协会(IFRA)实践法规要求或符...
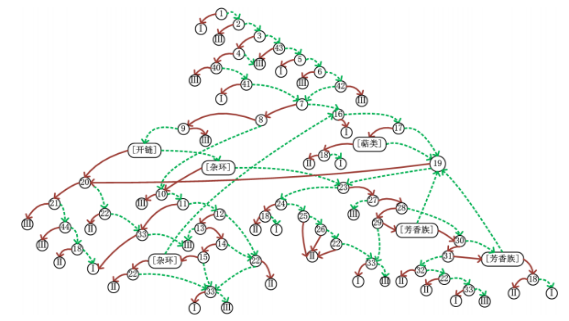
《交叉参照(Read-across)方法应用技术指南》
致敏性:根据供应商测试,局部封闭涂皮(BuehlerTest,BT)试验中,采用1 %的该原料进行诱导接触和激发接触,未见皮肤变态反应;遗传毒性:细菌回复突变试验和体外染色体畸变试验结果显示,未引起基因突变和染色体畸变;生殖发.....
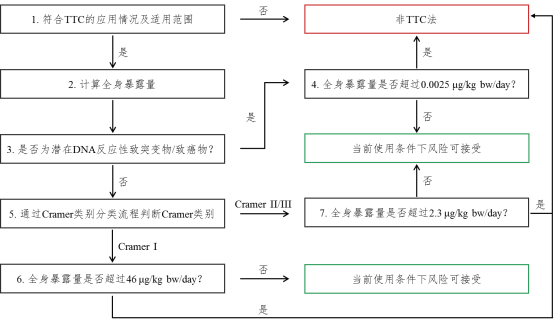
《毒理学关注阈值(TTC)方法应用技术指南》
致敏性:根据供应商测试,局部封闭涂皮(BuehlerTest,BT)试验中,采用0.1 %的该原料进行测试,未见皮肤变态反应;遗传毒性/DNA反应性终点:经细菌回复突变试验测试或软件(QSARToolbox和VEGA)预测并......
中检院关于公开征求《权威机构化妆品安全评估数据索引》等意见的通知
致敏性整合测试与评估策略应用技术指南(征求意见稿)》《权威机构化妆品安全评估数据索引(征求意见稿)》《化妆品原料使用信息(征求意见稿)》及其起草说明(附件1-7)。现向社会公开征求意见,请于2024年4月17日前将意见反馈表(附件8-10)...
中检院关于发布《化妆品安全评估资料提交指南(征求意见稿)》的通知
致敏性时,该原料用于化妆品是安全的”,可采用本产品的人体(满足伦理要求的前提下)或毒理学试验数据评估认为对消费者不具有刺激性/致敏性,采用该原料的评估结论。世界卫生组织(WHO)、联合国粮农组织(FAO)、欧洲食品安全局(EFSA)、欧洲药...
毒理学关注阈值(TTC)方法应用技术指南 (征求意见稿)
致敏性:根据供应商测试,局部封闭涂皮(BuehlerTest,BT)试验中,采用0.1%的该原料进行诱导接触和激发接触,未见皮肤变态反应;遗传毒性:细菌回复突变试验和体外染色体畸变试验结果显示,己基癸醇未引起基因突变和染色剂畸变;其他系.....