李锦聪|国产普通化妆品注册备案生产经营问答汇编
问:进行化妆品注册或备案申请时,送检样品是否可以用试制样品?
答:根据《化妆品注册和备案检验工作规范》第十一条“化妆品企业应当一次性向首家受理注册或备案检验申请的检验检测机构(以下简称首家检验检测机构)提供产品检验所需的全部样品。送检样品应当是包装完整且未启封的同一批号的市售样品,送检时尚未上市销售的产品,可以为试制样品。”
问:普通化妆品备案时,什么情况可以免于提交产品的毒理学试验报告?
答:根据《化妆品注册备案资料管理规定》第三十三条“普通化妆品的生产企业已取得所在国(地区)政府主管部门出具的生产质量管理体系相关资质认证,且产品安全风险评估结果能够充分确认产品安全性的,可免于提交该产品的毒理学试验报告,有下列情形的除外:
1.产品宣称婴幼儿和儿童使用的;
2.产品使用尚在安全监测中化妆品新原料的;
3.根据量化分级评分结果,备案人、境内责任人、生产企业被列为重点监管对象的。
有多个生产企业生产的,所有生产企业均已取得所在国(地区)政府主管部门出具的生产质量管理体系相关资质认证的,方可免于提交毒理学试验报告。”
问:多色号系列普通化妆品进行抽样毒理学试验的,申请备案时应注意哪些事项?
答:根据《化妆品注册备案资料管理规定》第三十三条要求“多色号系列普通化妆品按照《化妆品注册和备案检验工作规范》抽样进行毒理学试验的,可作为一组产品进行备案,每个产品均应附上系列产品的名单、基础配方和着色剂一览表以及抽检产品名单。”
问:需配合使用的普通化妆品,备案时如何开展毒理学试验?
答:根据《化妆品注册和备案检验工作规范》附件1《化妆品注册和备案检验项目要求》“毒理学试验、人体安全性与功效评价检验可按照说明书中使用方法进行检验;当存在各部分单独使用的可能性时,应当分别检验。”
问:多个生产企业生产同一普通化妆品的,该产品备案时检验报告如何提交?
答:根据《化妆品注册备案资料管理规定》第三十三条“多个生产企业生产同一产品的,应当提供其中一个生产企业样品完整的产品检验报告,并提交其他生产企业样品的微生物与理化检验报告。”
问:申请历史产品信息补充有什么要求?
答:按照国家药监局《化妆品注册备案信息服务平台使用常见问题解答》的相关要求,迁移至新系统的老产品,企业在完成信息补录操作时,现阶段仅有生产企业信息为补录时必填关联项,其他信息由企业自行决定是否在补录阶段提交。如为委托生产,需上传委托关系文件。按照国家药监局关于实施《化妆品注册备案资料管理规定》有关事项的公告(2021年第35号),在原注册备案平台已经完成备案的化妆品,备案人应当通过新注册备案平台,在2022年5月1日前提交产品执行的标准和产品标签样稿,填报国产普通化妆品的产品配方。
补录完成后方可进行产品变更。
问:完成历史产品信息补充之后进行备案变更时,仅提交涉及变更内容的资料是否可以?
答:不可以。完成历史产品信息补充之后进行备案变更时,需要按照《化妆品注册备案资料管理规定》的要求,提交全部备案资料。
问:现阶段产品安全评估资料有什么要求?
答:现阶段,备案人仍可按照《化妆品中可能存在的安全性风险物质风险评估指南》的要求开展风险评估,将风险评估资料上传到“产品安全评估”资料项下。
根据《国家药监局关于发布化妆品安全评估技术导则(2021年版)的公告》(2021年第51号),自2022年1月1日起,必须依据《技术导则》的要求开展化妆品安全评估,提交产品安全评估资料。
问:宣称祛痘、抗皱功效的淋洗类产品,提交了安全评估报告(简化版),是否可以免做人体试用试验安全性评价?
答:不可以。根据《化妆品注册备案资料管理规定》,宣称祛痘、抗皱功效的淋洗类产品,均应当进行人体试用试验安全性评价。进行人体安全性及功效评价检验之前,应当先完成微生物及理化检验、毒理学试验并出具书面报告,上述检验项目不合格的产品不得进行人体安全性评价检验。
问:在化妆品行政许可网上申报系统中取得进口非特殊用途化妆品行政许可批件的产品是否能将产品信息导入新的普通化妆品备案管理系统中?
答:不可以。在化妆品行政许可网上申报系统中取得进口非特殊用途化妆品行政许可批件的产品无法导入新的普通化妆品备案管理系统中。相关产品应按《化妆品注册备案管理办法》的相关要求进行备案。
问:普通化妆品备案管理系统进行产品注销是否要先进行补录?
答:根据系统最新公告,历史产品经确认后,可不进行补录操作,直接申请注销;已开始补录但未提交的历史产品,也可以申请注销。
问:由于企业的原因配方填报错误,是否可以申请配方变更?
答:按照《化妆品注册备案资料管理规定》,已备案的产品所使用原料的生产商、原料质量规格增加或者改变的,原料在配方中的含量和原料中主要功能成分含量及溶剂未发生变化,为了保证原料质量而添加的微量稳定剂、抗氧化剂、防腐剂等成分发生种类或者含量变化的,方可以变更。因企业自身原因配方填报错误请注销后重新备案。
问:普通化妆品是否可以使用苯乙基间苯二酚?
答:根据《国家食品药品监督管理局关于批准4-(1-苯乙基)-1,3-苯二酚作为化妆品原料使用的公告》(国家食药监局公告2012年第71号)批准苯乙基间苯二酚(商品名SymWhite®377)使用目的为:美白肌肤,通过抑制酪氨酸酶的活性抑制黑色素的形成。《化妆品注册备案管理办法》要求:“调整已使用的化妆品原料的使用目的、安全使用量等的,应当按照新原料注册、备案要求申请注册、进行备案。”
普通化妆品配方中若以其他使用目的添加苯乙基间苯二酚,应当按照新原料注册、备案要求完成注册或者备案。
问:化妆品用卡松原料系统填报卡松复配形式无溶剂是否合理?
答:卡松是化妆品中常见防腐剂,是甲基氯异噻唑啉酮和甲基异噻唑啉酮与氯化镁及硝酸镁的混合物,化妆品用的卡松通常为水溶液。根据《化妆品注册备案资料管理规定》要求:“产品配方应当提供全部原料的名称,原料名称包括标准中文名称、国际化妆品原料名称(简称INCI名称)或者英文名称。”卡松中如含有水或其他溶剂,应在配方中相应填报,确保配方表包含全部原料信息。
问:植物油如“甜扁桃油”在产品配方填报时是否需要注明具体提取部位?
答:植物油主要来自植物种子和果实,也有部分来自植物的叶、皮、根、花瓣和花蕊等。植物的提取形式比较复杂,由于其功效性和安全性是由其所含化学成分决定的,因此来源于不同器官(植物部位)的提取物,因其所含化学成分种类和含量的不同,会导致其功效性和安全性也存在差异,如苦参种子禁用,而苦参根可用。为明晰植物原料使用来源安全性,建议在配方填报时进行注明提取部位。
问:产品配方是**植物提取物,名称命名是否可以为**纯露?
答:根据纯露定义,纯露是指精油在蒸馏萃取过程中,在提炼精油时分离出来的一种100%饱和的蒸馏原液。植物提取物是指采用适当的溶剂或方法,以植物(植物全部或者某一部分)为原料提取或加工而成的物质。两者定义不同,制备方法、饱和度、原料中成分配比及含量等也不同。因此,植物提取物不能等同于纯露,使用**植物提取物作为原料时不宜命名为纯露。
问:化妆品标签是否可以宣称医疗研发机构和老字号医药品牌?
答:《化妆品监督管理条例》明确国家鼓励和支持开展化妆品研究、创新,满足消费者需求,推进化妆品品牌建设,发挥品牌引领作用。同时《化妆品标签管理办法》规定化妆品标签禁止利用国家机关、事业单位、医疗机构、公益性机构等单位及其工作人员、聘任的专家的名义、形象作证明或者推荐。企业应重视产品品质开发,致力于品牌建设,但不得利用医疗研发机构和老字号医药品牌暗示产品具有医疗作用,误导消费者。
问:产品执行的标准中微生物指标和理化指标质量控制措施中有“原料相关指标控制”描述的,简要说明未对“原料相关指标控制”进行具体解释。
答:按照《化妆品注册备案资料管理规定》要求“采用非检验方式作为质量控制措施的,应当明确具体的实施方案,对质量控制措施的合理性进行说明,以确保产品符合《化妆品安全技术规范》要求”,因此备案时应当在简要说明中解释“原料相关指标控制”的具体控制措施。《化妆品注册备案资料管理规定》附件16有“原料相关指标控制和全项检验”的举例说明(原料验收COA、必要的原料检验、具体的检验方法),备案人在实际填写时应依据申报产品的实际控制情况填写而不是简单照抄。
问:产品执行的标准中,微生物指标和理化指标质量管理措施中有“全项检验”“委托检验”描述的,未对检验频次进行说明。
答:按照《化妆品注册备案资料管理规定》要求“采用检验方式作为质量控制措施的,应当注明检验频次”,因此备案时应当在相应质量管理措施中注明检验频次。此外有“型式检验”等无法判断具体频次表述的,也应当明确具体检验频次。
问:普通化妆品(淋洗类发用产品除外)配方中添加了乳酸、柠檬酸……等α-羟基酸及其盐类和酯类且含量≥3%或者标签上宣称α-羟基酸时,产品执行的标准中质量控制措施仅设定α-羟基酸总量(以酸计)≤6%作为控制指标,不符合要求。
答:按照《化妆品注册备案资料管理规定》要求“应当根据产品实际控制的微生物和理化指标提交相应的控制措施”,因此应当根据产品配方实际添加α-羟基酸(及其盐类和酯类)种类和添加量进行具体控制,而不是将《化妆品安全技术规范》中的最大允许浓度作为控制指标。此外按照《化妆品注册和备案检验工作规范》、《化妆品安全技术规范》等法规要求该类产品还需要同时控制pH值并检测相关项目(纯油性含蜡基产品除外)。
问:产品配方中添加氢氧化钾、氢氧化钠、α-羟基酸(及其盐类和酯类)等《化妆品安全技术规范》中对pH值有限制和要求的成分,产品执行的标准中未体现对pH值进行控制。
答:按照《化妆品安全技术规范》要求产品配方中含有氢氧化钾、氢氧化钠、α-羟基酸(及其盐类和酯类)等在具体使用时有pH限制和要求的成分,应当在产品执行的标准中体现pH控制指标确保其满足法规要求。
问:普通化妆备案管理系统进行产品注销是否要先进行补录?
答:根据系统最新公告,历史产品经确认后,可不进行补录操作,直接发起注销申请;已开始补录但未提交的历史产品,也可发起注销申请。
问:原委托方未在普通化妆备案管理系统注册账号,之前备案的产品将如何处理?
答:根据国家药监局关于实施《化妆品注册备案资料管理规定》有关事项的公告 (2021年 第35号)要求:“自2022年1月1日起,通过原注册备案平台和新注册备案平台备案的普通化妆品,统一实施年度报告制度。备案人应当于每年1月1日至3月31日期间,通过新注册备案平台,提交备案时间满一年普通化妆品的年度报告。在原注册备案平台已经取得注册或者完成备案的化妆品,注册人、备案人应当通过新注册备案平台,在2022年5月1日前提交产品执行的标准和产品标签样稿、填报国产普通化妆品的产品配方、上传特殊化妆品销售包装的标签图片。”原委托方未注册账号,无法在新系统完成年报提交及补录工作,届时将根据相关要求进行处理。
问:企业在普通化妆品备案管理系统【历史产品确认】模块未发现历史产品,或缺失部分历史产品,如何处理?
答:(1)由于历史产品数据只会迁移到原委托方账号,企业可自查缺失的部分历史产品是否是作为受托生产企业进行备案;(2)系统历史产品数据是根据企业统一社会信用代码进行识别和关联,企业可自查新旧系统企业的统一信用代码是否一致;(3)如排除作为受托生产企业备案的产品及统一社会信用代码不一致的原因后,仍有缺失,可联系系统工作人员处理,联系方式:010-88331913或gcftba@nmpa.gov.cn
问:普通化妆品备案管理系统“产品执行的标准”模块,生产工艺中同一原料在不同步骤阶段中使用,应当如何区分?
答:通过在原料序号或者名称后标注“部分、剩余”的方式进行区分。如3号原料在步骤一和步骤二中使用,则在步骤一中标注“3(部分)”;步骤二中标注“3(剩余)”。
问:同一原料是否可以在普通化妆品备案管理系统产品配方表中分开填报?
答:原则上同一原料在普通化妆品备案管理系统配方表中不允许重复填报。但同一原料名称由于质量规格不同,可分开填报,须备注说明相应质量规格。
问:什么原料按照化妆品新原料进行管理?
答:根据《条例》规定,在我国境内首次使用于化妆品的天然或人工原料为化妆品新原料,经注册、备案的化妆品新原料纳入已使用化妆品原料目录前,仍然按照化妆品新原料进行管理。
应当注意的是,只有原料预期的使用方法、使用部位、使用目的符合化妆品的相关属性,才可以按照化妆品新原料申请注册或者进行备案。如某种原料发挥作用的使用方法是通过口服或者注射,不符合《条例》对化妆品使用方法的描述,即“涂擦、喷洒或者其他类似方法”,或者该原料的使用部位、使用目的不属于化妆品定义范畴的,则不能够按照化妆品新原料申请注册或进行备案。
同时,根据《规定》要求,化妆品新原料注册和备案资料应当以科学研究为基础,客观、准确地描述新原料的性状、特征和安全使用要求。申请注册或进行备案的化妆品新原料成分应当相对明确,注册人、备案人或境内责任人应当按要求提交化妆品新原料注册备案资料,并对所提交资料的合法性、真实性、准确性、完整性和可追溯性负责。
问:符合哪些情形的原料不属于化妆品新原料?
答:符合以下情形之一的原料,不属于化妆品新原料:
1.收录于《已使用化妆品原料目录(2021年版)》的原料。化妆品注册人、备案人在选用该目录中原料时,应当符合国家有关法律法规、强制性国家标准、技术规范的相关要求,并承担产品质量安全责任。如需超“最高历史使用量”使用时,应按照《化妆品安全评估技术导则》的程序和要求证明其安全性。
2.包含于已使用类别原料中的具体原料。如目录中已收载了类别原料“胶原”,即胶原蛋白,表示为某一类别原料的总称,该类别原料包含了不同工艺来源如动物组织提取、基因重组的胶原,也包含了不同分型如I型胶原、III型胶原等。此外,《已使用化妆品原料目录(2021版)》中收录的 “某某植物提取物”原料,例如“人参提取物”表示人参全株及其提取物均为已使用原料,若单独申报“人参汁”或者人参某个具体部位为新原料,则不予受理。
3.《化妆品安全技术规范》已规定为禁用组分的原料。如人的细胞、组织或人源产品;抗组胺药物;激素类物质等。
4.实际功能超出化妆品的定义范畴的原料。如具有“激活细胞”“再生细胞”“降低伤口部位的色素沉积”“促愈合作用”“促进重金属外排” 等具有医疗作用的原料。
问:如何正确理解化妆品新原料备案?
答:根据《条例》规定,国家按照风险程度对化妆品原料实行分类管理,对风险程度较高的化妆品新原料实行注册管理,对其他化妆品新原料实行备案管理。化妆品新原料备案人通过国务院药品监督管理部门在线政务服务平台提交本条例规定的备案资料后即完成备案。
备案的真实含义是新原料备案人向药品监管部门提交资料备查。化妆品新原料备案人完成备案后,国家药监局公布新原料备案信息,仅代表该原料已完成备案资料的提交,符合形式要求,而对其资料内容的真实性、科学性、充分性可能尚未核查。公开已完成备案的化妆品新原料相关信息不代表认可该新原料的安全性与功能性,更无所谓的“成功获得批准备案”的说法。
根据《条例》《办法》规定,化妆品新原料完成备案后,药品监督管理部门将组织技术审评机构对新原料的备案资料开展技术核查,并对化妆品新原料的使用和安全情况进行跟踪评估,发现已备案化妆品新原料的备案资料不符合要求的,将责令限期改正,其中,与化妆品新原料安全性有关的备案资料不符合要求的,可以同时责令暂停新原料的销售、使用;发现化妆品新原料不属于备案范围,或者备案时提交虚假资料等问题的,将取消化妆品新原料的备案;化妆品新原料被责令暂停使用或者取消备案,化妆品注册人、备案人应当同时暂停或者停止生产、经营使用该新原料的化妆品。
问:新原料完成注册备案后,化妆品新原料注册人、备案人还应当履行哪些义务?
答:根据《条例》《办法》规定,化妆品新原料注册人、备案人对化妆品新原料的质量安全负责。已经取得注册、完成备案的化妆品新原料实行安全监测期制度,安全监测期内,化妆品新原料注册人、备案人应当密切关注新原料的安全使用情况,按照《规定》要求收集、整理新原料使用相关信息资料,编制《化妆品新原料安全监测年度报告》,在化妆品新原料安全监测每满一年前30个工作日内,通过信息服务平台向技术审评机构提交。
如化妆品新原料注册人、备案人发现新原料使用过程中存在《办法》规定应当向技术审评机构报告的情况,或其他认为需要报告的情形,应当立即按照《规定》要求编制《化妆品新原料安全风险控制报告》,通过信息服务平台向技术审评机构提交。
问:如何根据化妆品新原料的属性,判定化妆品新原料应当申请注册或进行备案?
答:根据《条例》规定,具有防腐、防晒、着色、染发、祛斑美白功能的化妆品新原料,经国务院药品监督管理部门注册后方可使用;其他化妆品新原料应当在使用前向国务院药品监督管理部门备案。这是基于风险管理的原则,对相对较高风险的几类原料实行注册管理,其他原料实行备案管理。在化妆品新原料研发过程中,往往发现某一个新原料可能同时具有多种功能。化妆品新原料注册人、备案人在申请注册或进行备案前,应当对新原料可能具有的实际功能进行全面梳理和充分研究,科学、合理地作出该种新原料是否属于应当申报注册情形的判断。
一般而言,对同时具有多种功能的新原料,只要其中某一功能属于应当申报注册的情形,该新原料就应当按照《规定》要求申报注册,经批准注册后方可使用;如果同时具有的多种功能均不属于应当申报注册的情形,无论功能种类多少,在使用前按照《规定》要求向国家药监局进行备案即可。化妆品新原料注册人、备案人不得故意隐瞒新原料实际具有的功能,不得对应当申报注册的化妆品新原料仅仅进行备案后便用于化妆品生产。此种行为一经查实,将依照《条例》第五十九条第三项的规定进行处罚。
问:质量安全负责人能否在不同的化妆品注册人、备案人、受托生产企业兼任?
答:为保障化妆品质量安全,确保质量安全负责人依法落实产品质量安全管理和产品放行职责,按照“一证一人”的原则,申请两个以上(含两个)的化妆品生产许可,不得由同一个自然人担任上述企业的质量安全负责人;不同的化妆品注册人、备案人,不得由同一个自然人担任质量安全负责人。化妆品注册人、备案人与受托生产企业属于同一集团公司,执行同一质量管理体系,受托生产企业接受该注册人、备案人的委托生产化妆品时,该注册人、备案人与受托生产企业可以聘用同一个自然人担任质量安全负责人。
问:质量安全负责人可否授权他人代为履行其职责?
答:《办法》第二十八条规定,质量安全负责人按照化妆品质量安全责任制的要求协助化妆品注册人、备案人、受托生产企业法定代表人、主要负责人承担相应的产品质量安全管理和产品放行职责。根据化妆品注册人、备案人、受托生产企业生产质量管理体系运行需要,经法定代表人或者主要负责人书面同意,质量安全负责人可以授权他人代为履行其职责。被授权人应当具有相应资质和履职能力。质量安全负责人授权的时间、授权的人员、授权的事项等应当如实记录,确保授权行为可追溯。质量安全负责人应当对被授权人履行职责情况进行监督,且其应当承担的法律责任并不转移给被授权人。
问:如何正确理解“标注标签的生产工序,应当在完成最后一道接触化妆品内容物生产工序的化妆品生产企业内完成”?
答:《办法》第六十三条规定,化妆品标注标签的生产工序,应当在完成最后一道接触化妆品内容物生产工序的化妆品生产企业内完成。该条款立法原意是禁止化妆品在完成产品标签标注前出厂,导致产品无法追溯。该条款中“化妆品标注标签的生产工序”,是指在接触化妆品内容物的包装材料上标注标签的生产工序。值得注意的是,进口化妆品在其原包装标注标签的生产工序已经完成并可追溯的前提下,加贴中文标签的行为可以不在完成最后一道接触化妆品内容物生产工序的化妆品生产企业内完成。
问:直接从事化妆品生产活动的人员包括哪些?国务院卫生主管部门规定的有碍化妆品质量安全的疾病有哪些?
答:《条例》规定的“直接从事化妆品生产活动的人员”的范围,根据实际情况确定,原则上应当包括从事化妆品生产、检验和仓库相关操作人员等。此类从业人员入职前和在岗期间应当按规定进行健康检查,取得医疗机构出具的检查项目齐全并有明确结论的体检报告后方能上岗。
依据《条例》规定,由国务院卫生主管部门规定有碍化妆品质量安全疾病的范围。在国务院卫生主管部门出台有关规定之前,目前执行原法规《化妆品卫生监督条例》规定的有碍化妆品质量安全疾病的范围,包括:痢疾、伤寒、病毒性肝炎、活动性肺结核、手部皮肤病(手癣、指甲癣、手部湿疹、发生于手部的银屑病或者鳞屑)和渗出性皮肤病等疾病。患有这些疾病的人员,不能直接从事化妆品生产活动。
问:化妆品经营者是否应当建立并执行产品销售记录制度?
答:依据《条例》和《办法》的规定,化妆品注册人、备案人、受托生产企业应当建立并执行产品销售记录制度。商场、超市等化妆品经营者不强制建立并执行产品销售记录制度,但应当采取有效措施确保产品可追溯。如化妆品经营者的销售对象为其他化妆品经营者,鼓励其建立并执行产品销售记录制度。
问:美容美发机构、宾馆等是否可以配制、灌装化妆品?
答:美容美发机构、宾馆等在经营中使用化妆品或者为消费者提供化妆品的,应当依法履行《条例》以及《办法》规定的化妆品经营者义务,其为消费者提供的化妆品应当符合最小销售单元标签的规定。
按照《办法》规定,配制、填充、灌装化妆品内容物,应当取得化妆品生产许可证。美容美发机构等不得自行配制化妆品,也不得擅自填充、灌装化妆品内容物,但依照化妆品标签或者说明书中使用方法,现场调配化妆品给消费者使用的情形除外。宾馆、洗浴中心、婚纱影楼、月子中心等为消费者提供的化妆品应当有符合规定的产品标签,标签应当标注产品名称、特殊化妆品注册证编号,注册人、备案人、受托生产企业的名称、地址,化妆品生产许可证编号,产品执行的标准编号,全成分,净含量,使用期限、使用方法以及必要的安全警示,以及法律、行政法规和强制性国家标准规定应当标注的其他内容。
问:化妆品是否可以标注“刷酸”?
答:“刷酸”所使用的“酸”并不是化妆品,且“刷酸”时“酸”的浓度一般相对较高,远高于化妆品对“酸”类原料的限量要求,因此,应避免使用“刷酸”等不当宣称。
《国家药监局关于开展化妆品“线上净网线下清源”专项行动的通知》(国药监妆〔2021〕47号)要求对违法宣称药妆、干细胞、刷酸、医学护肤品的化妆品进行清理整治。“刷酸”被列为虚假或引人误解,明示或暗示具有医疗作用的内容。
问:普通化妆品中添加化学防晒剂有哪些注意事项?
答:非防晒类产品提交配方中使用化学防晒剂的,应当检测所含化学防晒剂;化学防晒剂含量≥0.5%(w/w)的产品(淋洗类、香水类、指甲油类除外),除规定项目外,还应进行皮肤光毒性试验、皮肤变态反应试验和检测SPF值;化学防晒剂的使用目的根据产品实际,可为“稳定剂”或“产品保护剂”,不能用作“皮肤调理剂”。
问:企业备案人、生产企业名称带有“李时珍国药”“**制药”等涉及医疗词语是否可以标注?
答:“李时珍国药”“**制药”等作为备案人、生产企业名称的一部分,未做强调性标注时可在产品包装上正常标注。但不能在产品包装上采取有意着重、强调的方式进行标注。同时“李时珍国药”“**制药”等不能作为注册商标名出现在产品名称,涉嫌产品名称或宣称中使用医疗术语。
问:普通化妆品备案对上传的平面图和立体图有什么要求?
答:备案上传的平面图、立体图应为市售包装图,也可以是与实物一致的效果图,但不能是标注色泽和尺寸等信息的设计图。平面图应包含产品所有可视面,圆柱型、球状体等异型包装应局部拍照确保边缘处及光影处字迹信息清晰可辨识。
问:配方中只含有氨基酸表活,如椰油酰甘氨酸钠、月桂酰谷氨酸二钠、月桂酰肌氨酸钠等,是否可以宣称氨基酸?
答:《化妆品标签管理办法》规定:“使用具体原料名称或者表明原料类别的词汇的,应当与产品配方成分相符,且该原料在产品中产生的功效作用应当与产品功效宣称相符”。宣称“氨基酸”与配方中“氨基酸表活”成分不符,二者功效作用也不相同。
问:新备案平台临时用户权限是指什么?
答:已经通过旧平台取得注册或者完成备案的化妆品企业,由于质量管理体系、不良反应监测和评价体系尚在整理完善过程中,在新平台申请用户时暂时无法提交注册人、备案人的质量管理体系概述、不良反应监测和评价体系概述等资料的,各省局可以对其用户申请有条件审核通过,开通临时用户权限,允许其开展化妆品注册备案相关工作。
问:新备案平台临时用户权限是否有期限?
答:已开通新平台临时用户权限的化妆品注册人、备案人、境内责任人,应当于2022年1月1日前补充提交质量管理体系概述、不良反应监测和评价体系概述等资料,逾期未补充提交的,其临时用户权限自2022年1月1日起自动失效。待相关资料整理完成后,后续仍可申请开通注册备案用户权限。
问:旧系统产品补录需提交哪些资料?
答:国家药监局关于实施《化妆品注册备案资料管理规定》有关事项的公告(2021年 第35号)规定:在原注册备案平台已经取得注册或者完成备案的化妆品,注册人、备案人应当通过新注册备案平台,在2022年5月1日前提交产品执行的标准和产品标签样稿、填报国产普通化妆品的产品配方、上传特殊化妆品销售包装的标签图片。
问:哪些操作前需要进行历史产品信息补充?
答:根据国家药品监督管理局发布的《化妆品注册备案信息服务平台上线通知》中的操作指引,普通化妆品备案管理平台在进行“备案变更”“产品年度报告”和“备案注销”等操作前,需要先进行“历史产品信息补充”。建议对迁移至新系统的产品尽快进行“历史产品信息补充”,以免影响产品后续的“产品年度报告”等操作。
问:《已使用化妆品原料目录(2021版)》已经施行,现在补录是否需要按照2021版补录配方?如果按照2021版目录制作补录配方,会造成备案成分的表述与实际包装不一致,是否有问题?
答:国家药品监督管理局发布的《已使用化妆品原料目录(2021年版)》公告(2021年 第62号)规定《已使用化妆品原料目录(2021年版)》自2021年5月1日起施行。如产品同一原料由于新旧目录的名称不同导致不符合《已使用化妆品原料目录(2021年版)》要求,须及时进行产品变更,且产品标签须与系统配方保持一致。
问:普通化妆品备案对注册商标使用的要求?
答:根据《化妆品命名规定》、《化妆品标签管理办法》、《化妆品注册备案资料管理规定》,产品中文名称中的注册商标使用字母、汉语拼音、数字、符号等的,应当在产品销售包装可视面对其含义予以解释说明,并应当提供商标注册证。
化妆品商标名的使用应当符合国家化妆品管理相关法律法规的规定,还应当符合国家有关商标管理法律法规的规定。依据《商标法》及《商标法实施条例》的有关规定,未经商标注册人的许可,在同一种商品上使用与其注册商标相同的商标的,属侵犯注册商标专用权行为。商标注册人可以通过签订商标使用许可合同,许可他人使用其注册商标。
化妆品备案人对化妆品标签的合法性、真实性、完整性、准确性和一致性负责。对产品使用他人“注册商标”的情况,备案前应先取得商标注册人许可,许可合同可作为备案必须提交资料,但备案人应保证合法性并存档备查。
问:产品功效依据是否允许企业依据行业标准或者团体标准或企业标准?
答:《化妆品功效宣称评价规范》第十五条规定:除有特殊规定的情形外,化妆品功效宣称评价试验应当优先选择下列(一)(二)项试验方法,(一)(二)项未作规定的,可以任意选择下列(三)(四)项试验方法:(一)我国化妆品强制性国家标准、技术规范规定的方法;(二)我国其他相关法规、国家标准、行业标准载明的方法;(三)国外相关法规或技术标准规定的方法;(四)国内外权威组织、技术机构以及行业协会技术指南发布的方法、专业学术杂志、期刊公开发表的方法或自行拟定建立的方法,在开展功效评价前,评价机构应当完成必要的试验方法转移、确认或验证,以确保评价工作的科学性、可靠性。
问:安评报告中,原料毒理安全数据的来源有哪些?
答:《化妆品安全评估技术导则(2021年版)》规定:化妆品产品安全评估报告(简化版)可采用的证据有《化妆品安全技术规范》要求、权威机构评估结论、企业原料历史使用量和《已使用原料目录(2021版)》中的最高历史使用量。安评报告引用的相关数据出处及来源在“参考文献”按照格式要求明确列出。化妆品注册人、备案人应自行或委托专业机构开展安全评估,形成安全评估报告,并对其真实性、科学性负责。
问:同一种原料生产商应该填报一家还是可以多家?
答:同一种原料的生产商需根据该原料质量规格填报,多家生产商的原料质量规格一致,可填报多家,如果不一致,则需分别填报。
问:旧系统产品配方其中一种原料是复配原料,在历史备案中填写的是单一成分,企业补录产品是否可以按实际成分填报?
答:《化妆品注册备案资料管理规定》第四十二条规定已注册或者备案产品所使用原料的生产商、原料质量规格增加或者改变的,所使用的原料在配方中的含量以及原料中具体成分的种类、比例均未发生变化的,应当通过注册备案信息平台对原料生产商信息和原料安全信息进行更新维护。涉及产品安全评估资料发生变化的,还应当进行产品安全评估资料变更。
已注册或者备案产品所使用原料的生产商、原料质量规格增加或者改变的,原料在配方中的含量和原料中主要功能成分含量及溶剂未发生变化,为了保证原料质量而添加的微量稳定剂、抗氧化剂、防腐剂等成分发生种类或者含量变化的,应当提交相应资料。
问:补录产品包装是否可以按新标签管理办法要求进行内容修改?
答:国家药监局关于发布实施《化妆品标签管理办法》的公告(2021年第77号)规定鼓励化妆品注册人、备案人自本公告发布之日起,按照《办法》规定对化妆品进行标签标识。补录产品包装可按新标签管理办法要求进行修改。
问:旧备案系统9月15日关闭有哪些影响?
答:按照《国家药监局关于做好新旧化妆品注册备案信息管理平台衔接有关工作事项的通知》,责令整改的产品,需在9月15日之前完成整改提交。9月15日后,老系统将停止企业端服务,并逐步将老系统产品的最新状态数据迁移至新平台进行公开。新平台公开前,老系统的查询服务不会停。
1、9月15日是国产非特殊用户化妆品备案系统备案后检查截止日期,非系统关闭时间;
2、服务平台中的公示信息,会在关闭前切换到新系统的公示平台进行公示;
3、国家局尚未通知国产非特殊用户化妆品备案系统及服务平台关闭时间,如关闭,会提前在国家局官网中发布公告信息。
问:普通化妆品备案要多长时间?
答:根据《化妆品监督管理条例》第二十条规定:普通化妆品备案人通过国务院药品监督管理部门在线政务服务平台提交本条例规定的备案资料后即完成备案。省级以上人民政府药品监督管理部门应当自特殊化妆品准予注册之日起、普通化妆品备案人提交备案资料之日起5个工作日内向社会公布注册、备案有关信息。
问:近期新的备案系统问题出现很多问题,应该如何联系备案系统人员?
答:企业信息资料管理、普通化妆品备案咨询电话:010-88331913;邮箱:gcftba@nmpa.gov.cn
化妆品智慧申报审评咨询电话:010-883636828;邮箱:hukang@nifdc.org.cn
问:备案检验报告是否有“有效期”?
答:现行《国家药监局关于发布实施化妆品注册和备案检验工作规范的公告》(2019年第72号)未规定检验报告有效期。原国家食品药品监督管理局《关于印发化妆品行政许可检验管理办法的通知》(国食药监许〔2010〕82号)中检验报告体例声明“本检验报告自出具之日起二年内有效”,我们认为是指取得备案检验报告后应该在两年内办理备案。
问:0.1%含量的成分属于微量成分吗?
答:《化妆品标签管理办法》 第十二条规定:化妆品配方中存在含量不超过0.1%(w/w)的成分的,所有不超过0.1%(w/w)的成分应当以“其他微量成分”作为引导语引出另行标注,可以不按照成分含量的降序列出。因此,0.1%含量的成分属于“其他微量成分”。
问:系统提示“有新原料没有被发送授权申请信息”,该怎么处理?
答:如产品未使用新原料,无需在“使用已注册新原料”“使用已备案新原料”选项里填写任何内容,如“/”等,否则系统将提示“有新原料没有被发送授权申请信息”。
问:新系统备案操作过程中出现页面响应,是什么问题?
答:浏览器都有个缓存上线,备案信息量过大,浏览器释放缓存的速度赶不上打开备案信息的速度,内存只增加不释放,浏览器即会提示无响应。建议使用缓存较大的谷歌和火狐浏览器。
问:为什么点击提交系统将提示“未上传备案信息表”?
答:企业提交备案时,需注意在“产品安全评估”页面的“附件上传”菜单中,上传系统生成并由企业盖章后的“备案信息表”,否则系统将提示“未上传备案信息表”。
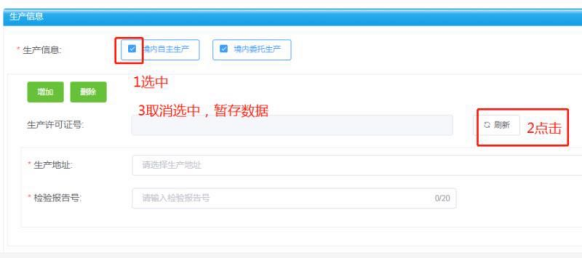
问:企业信息变更后,产品备案信息里的企业信息仍显示变更前信息,该如何操作?
答:确认企业信息已变更通过的情况下:1、勾选中“生产信息”栏里的“境内自主生产”;2、点击“刷新”;3、取消步骤1选中,暂存数据,详见图解。
问:备案人既自主生产又受托生产,是否需要开通生产企业角色?
答:办理仅供出口产品备案需开通生产企业角色。备案人如果不涉及办理仅供出口产品备案则不需要开通生产企业角色,受托关联可在备案人角色确认。
问:备案资料提交时怎么显示“错误原因:请联系管理员,系统未找到当前用户的审核人!”?
答:每个产品的备案申请单需由同一账号完成编辑提交,如多个经办人账号参与编辑,在提交时会提示错误。
问:新系统中进行老产品变更应该注意什么?
答:迁移至新系统的老产品,企业在完成信息补录操作后,方可进行产品变更。(现阶段仅有生产企业信息为补录时必填关联项,其他信息由企业自行决定是否在补录阶段提交)
问:尚未公布的普通化妆品备案信息如何主动增补、修改资料?
答:根据《化妆品监督管理条例》、《化妆品注册备案管理办法》规定,普通化妆品备案人提交备案资料即完成备案,产品可上市销售。近期有部分化妆品备案人咨询,化妆品备案资料提交后,在备案资料信息公布前,备案人自主检查发现资料漏报或填错,如何进行撤回备案并补充修改。
当前化妆品备案信息服务平台未设置“退回”功能,为提高备案工作效率,现采取临时措施:如备案人遇到上述原因需要申请撤回备案的情况,请备案人填写《广州市普通化妆品备案资料撤回修改申请表》,将申请表word版及加盖公章后的扫描版发邮件至备案咨询邮箱:ft@qmark.com.cn。广州市市场监督管理局收到申请表,核实备案人申请后2个工作日内通过“责令改正”方式退回备案人,其修改后重新提交。
问:化妆品注册备案信息服务平台如何使用?
答:较之前旧备案信息管理系统直接在系统上完成账号注册和产品备案操作不同,今年5月1日起启用的化妆品注册备案平台使用需进行三个步骤:1、访问国家药监局网上办事大厅注册法人账号和/或经办人账号;2、访问企业信息资料管理系统,申办注册人/备案人、境内责任人、生产企业角色权限。3、访问普通化妆品备案管理系统进行新产品备案、已有产品补录、备案变更、备案注销及产品年度报告。
由于近期化妆品注册备案平台刚投入使用,咨询量较大,为更加快捷、精确的收集与记录问题,提高问题处理效率,建议大家采用以下方式解决使用问题:
1.参考系统操作手册、常见问题解答自行排查。系统将加紧处理企业反映的问题,对已解决的共性问题会通过及时更新操作手册、常见问题解答相关内容,来协助企业解决在系统使用过程中出现的普遍问题,建议仔细阅读。
2.优先选择咨询邮箱进行反馈。如果操作手册及问题解答仍未解决您的问题,请将问题反馈至邮箱,邮件中请尽量详细描述遇到的问题,并附操作截图及联系方式等,系统工作人员将会优先处理和解答。
3.企业信息资料管理系统操作手册下载链接:https://hzpba.nmpa.gov.cn/YHGL/qyxxzl.pdf
4.普通化妆品备案管理操作手册下载链接:https://hzpba.nmpa.gov.cn/PTHZPBA/pthzpba.pdf
5.常见问题解答链:https://hzpba.nmpa.gov.cn/YHGL/faq.html
6.咨询邮箱:gcftba@nmpa.gov.cn
7.咨询电话:010-88331913
问:因历史原因,检验报告送检人与产品注册人备案人不一致的情况如何处理?
答:因历史原因,对检验报告送检人与产品注册人备案人不一致的检验报告,在产品注册备案时注册人备案人自行上传检验报告的同时,增加上传产品注册人备案人出具的委托送检的证明函件原件扫描件。
问:产品存在多个注册商标,新注册备案平台如何提交?
答:产品存在多个注册商标的,合并在一个文档中上传。
问:产品被责改修改后提交时提示:“错误原因:备案申请提交失败!提交人与首次填报人不是同一人。”,该如何处理?
答:产品被责改修改后提交人需与首次填报人保持一致。如出现该提示,企业可删除备案申请,重新填报资料后再次提交备案申请。
问:产品配方导入后配方怎么出现乱码?
答:注册人备案人上传产品配方时,确认excel文档中不包含公示计算。如排除文档中不含公示计算,可提供具体产品信息,发邮件至系统邮箱做进一步原因分析。系统邮箱:gcftba@nmpa.gov.cn
问:新注册备案平台新注册账号如何获取检验系统账号
答:新注册备案平台注册备案人完成注册备案人角色申请通过后,进入化妆品注册和备案检验信息管理系统,选择企业登录>找回密码,“账号”填报社会统一信用代码的9-17位,“邮箱”是企业申请注册备案人角色时填报的联系人对应邮箱。点击发送邮件后,通过邮件连接进行密码设置。
问:产品备案资料提交后在未公示之前是否可以进行变更操作?
答:产品备案资料提交完成需在监管端完成“资料整理”环节之后才可以进行变更操作。
问:旧系统已备案产品在新注册备案平台“历史产品确认”里点击“确认”后,在“历史产品信息补充”里没找到,是需要等核查吗?
答:历史产品确认不需要核查。这种情况可选择“新增”,输入备案编号后,点“确定”找到历史产品。
问:产品因变更需要在“历史产品信息补充”进行基础信息补录后,后续按法规要求补齐其余资料是否依然在“历史产品信息补充”进行?
答:“历史产品信息补充”只能进行一次信息补充,后续其余资料补齐操作可在“备案变更”操作进行。
问:旧系统委托方完成了备案后检查,受托方备案后检查被责令整改,委托方是否可以继续在旧系统进行变更修改?
答:备案产品受托方被责改的,委托方无法在老系统申请变更,只有委托方被责改的才能在老系统变更。这种情况建议在新注册备案平台进行变更。
问:化妆品标签中的商标使用需要符合哪些规定?
答:《化妆品标签管理办法》第四条规定“化妆品注册人、备案人对化妆品标签的合法性、真实性、完整性、准确性和一致性负责”和第八条第一款规定“商标名的使用除符合国家商标有关法律法规的规定外,还应当符合国家化妆品管理相关法律法规的规定”。同时《化妆品注册备案资料管理规定》第二十八条规定“产品中文名称中商标名使用字母、汉语拼音、数字、符号等的,应当提供商标注册证”。
问:备案产品已从旧系统迁移到新系统,现在需要注销重新备案,需要历史产品确认补录后再注销吗?
答:可选择在旧系统注销,注销信息会定期同步到新系统。也可以选择新系统注销,则需要先进行补录再操作注销。
问:已开通新系统账号,现在该企业已注销,是在化妆品注册备案平台“企业信息资料管理”注销企业账号吗?还是在办事大厅注销?如账号注销,该账号下原已备案的所有产品信息是否跟着全部注销?
答:是在化妆品注册备案平台企业信息资料管理注销账号,注销后该企业的所有产品也会自动注销。
问:燕麦(AVENA SATIVA)β-葡聚糖这个成分本身就没有INCI名称,上传配方表提示不能为空。该如何处理?
答:在配方导入模板“INCI名称”一栏可用文字填上后再导入,然后在系统“产品配方”界面上将该成分“INCI名称”一栏中的文字删除。
问:原料中成分含量为何显示空白?
答:一般是由于输入带“%”号的数值导致的,只需要录入数值。
问:如何取得化妆品注册备案信息服务平台用户?
答:根据《规定》要求,境内的注册人、备案人、境内责任人和化妆品生产企业应当通过注册备案信息服务平台取得化妆品注册备案用户后,方可办理化妆品注册备案。境外的注册人、备案人,通过其境内责任人的用户开展化妆品注册备案相关业务。
《条例》第十八条对化妆品注册人、备案人的要求是一致的,符合要求的企业或者其他组织提交相关资料一并开通注册人和备案人用户后,即可开展化妆品注册、备案相关工作,不需要分别开通注册人、备案人权限。
问:哪些化妆品注册人、备案人需要指定境内责任人?
答:化妆品注册人、备案人在境外的,应当在我国境内指定境内责任人,办理化妆品注册备案,协助开展化妆品不良反应监测、实施产品召回。
境外注册人、备案人委托境内化妆品生产企业生产化妆品的,该化妆品为国产化妆品,但由于注册人、备案人在境外,需要指定境内责任人;境内注册人、备案人委托境外化妆品生产企业生产化妆品的,该化妆品为进口化妆品,但由于注册人、备案人在境内,不需要指定境内责任人。
问:境内责任人与原在华申报责任单位有哪些区别?
答:境内责任人与原《化妆品卫生监督管理条例》及相关法规规定中的在华申报责任单位相比,不仅需要以注册人、备案人的名义办理注册、备案,还需要履行协助开展不良反应监测、实施产品召回、按照协议承担相应的质量安全责任等义务。
在华申报责任单位如果不具备履行境内责任人相应义务能力的,不能作为境内责任人开展化妆品的注册备案工作。
问:境内责任人授权书需要载明哪些内容?
答:境内责任人授权书内容应当至少体现以下内容和信息:注册人、备案人和境内责任人名称,授权和被授权关系,授权范围,授权期限。
授权期限不明确的,视为永久授权;无论授权书是否体现协助开展化妆品不良反应监测、实施产品召回和配合监督检查等内容,境内责任人均应当按照法规要求履行协助开展不良反应监测、实施产品召回和配合监督检查等义务。
问:境内责任人的授权书能否使用原授权书?
答:原进口特殊化妆品在华申报责任单位授权书,不能继续使用。原进口普通化妆品的境内责任人授权书,可以继续使用(仅办理普通化妆品进口备案)。因原境内责任人授权书此前已提交受理部门无法再次提供原件的,境内责任人在开通境内责任人用户时应当通过注册备案信息服务平台上传授权书原件扫描件,提交纸质文件时可提交授权书复印件。
境外注册人、备案人拟扩大原境内责任人授权办理范围的,应当重新出具授权书。境内责任人可以先通过注册备案信息服务平台上传新授权书原件扫描件办理化妆品注册备案用户,并应当于2021年9月30日前补充提交授权书原件及其公证件等资料。
问:使用了安全监测期新原料的化妆品如何注册、备案?
答:化妆品新原料取得注册、进行备案后,国家药监局会向社会公布新原料注册、备案管理相关信息。其他化妆品注册人、备案人使用新原料生产化妆品的,应当在化妆品办理注册、备案时填写新原料注册、备案编号,通过注册备案信息服务平台经新原料注册人、备案人关联确认,方可提交注册申请、备案资料。
使用了安全监测期新原料生产化妆品的化妆品注册人、备案人,应当按照《办法》规定要求履行新原料使用和安全情况监测义务。
问:新原料被责令暂停使用,相关化妆品如何处置?
答:安全监测期内的化妆品新原料被责令暂停使用的,注册备案信息服务平台会自动识别使用该新原料的化妆品并给予提示,相关化妆品注册人、备案人应当同时暂停生产、经营使用该新原料的化妆品。
问:存在委托生产情形的化妆品如何办理注册、备案?
答:化妆品注册人、备案人委托生产国产化妆品的,化妆品注册人、备案人或者境内责任人应当通过注册备案信息服务平台经化妆品生产企业确认委托生产关系后,方可提交注册申请、进行备案;化妆品注册人、备案人委托生产进口化妆品的,化妆品注册人、备案人或者境内责任人应当在申请注册、进行备案时,提交证明委托生产关系的相关材料。
问:化妆品注册人、备案人如何留样?
答:《规定》第三十六条规定,化妆品注册人备案人应当留存每一批生产的化妆品样品备查。留存样品数量应当能够满足开展注册备案检验所需,可以不包括防晒、祛斑美白、防脱发等人体功效试验所需的样品数量。
问:必须配合仪器或工具使用的化妆品如何注册备案?
答:除仅辅助涂擦的毛刷、气垫、烫发工具等外,必须配合仪器或者工具使用的化妆品,其产品安全评估过程中应当评估配合仪器或者工具使用条件下的安全性。
原则上,配合使用的仪器或者工具,不应具有化妆品功能,不应参与化妆品的再生产过程,不能改变化妆品与皮肤的作用方式和作用机理。
问:化妆品配方是否允许变更?
答:已注册备案化妆品的配方不允许变更。根据《办法》和《规定》,已注册、备案的化妆品,因其使用的原料更换供应商等导致产品配方不可避免的发生微小变化,这种情形的配方微小变化是允许的,但应当履行《办法》和《规定》规定的义务。但除此情形之外的产品配方变化,实质上构成了新产品,应当重新申请注册、进行备案。
问:普通化妆品的备案管理部门改变如何处理?
答:普通化妆品备案人、境内责任人地址跨省份发生变化,导致备案管理部门改变的,普通化妆品的备案编号和备案监管责任也会发生改变,因此需要重新进行备案。重新进行备案时仍可使用原备案资料,注册备案信息服务平台也会设置相应功能,方便备案人、境内责任人重新进行备案。
问:化妆品功效宣称依据的摘要需要填报哪些内容?
答:根据《化妆品功效宣称评价规范》第十九条规定:化妆品功效宣称依据的摘要应当简明扼要地列出产品功效宣称依据的内容,至少包括以下信息:
(一)产品基本信息;
(二)功效宣称评价项目及评价机构;
(三)评价方法与结果简述;
(四)功效宣称评价结论,应当阐明产品的功效宣称与评价方法与结果之间的关联性。
问:能够通过感官直接识别或仅通过物理方式发生效果的化妆品如何在备案系统上操作免予公布产品功效宣称依据的摘要?
答:根据《化妆品功效宣称评价规范》第四条规定:化妆品注册人、备案人在申请注册或进行备案的同时,应当按照本规范要求,在国家药品监督管理局指定的专门网站上传产品功效宣称依据的摘要。
免予公布产品功效宣称依据的摘要的产品需要在普通化妆品备案管理系统中的“功效宣称”模块进行产品功效宣称填报,根据产品的分类编码,在“产品功效宣称”项目填报功效名称,并在“是否免予”一栏勾选“是”,“备注”栏将自动显示“根据《化妆品功效宣称评价规范》,能够通过视觉、嗅觉等感官直接识别的,可免予公布产品功效宣称依据的摘要”的说明,然后提交功效宣称。
问:功效宣称摘要填报错误是否可以撤回修改?
答:功效宣称摘要资料提交后无法撤回,备案人可以再次编写功效宣称摘要资料重新提交,公示系统将公示最新提交的功效宣称摘要内容。备案人所有提交的功效宣称摘要资料将留存系统备查。
问:化妆品原料安全信息登记平台上线后是否只能通过原料报送码关联原料信息?
答:化妆品原料安全信息登记平台上线后,化妆品注册人、备案人、境内责任人仍可以通过化妆品注册备案信息服务平台填报原料生产商出具的原料安全信息文件,也可以填写化妆品原料安全信息登记平台生成的原料报送码关联原料安全信息文件。
问:如何规范填报化妆品备案产品名称命名依据?
答:根据《化妆品注册备案资料管理规定》第二十八条规定:“注册人、备案人应当提交产品名称命名依据,产品名称命名依据中应当指明商标名、通用名、属性名,并分别说明其具体含义”。
示例:GZcosmetics滋润保湿面霜
| 产品名称命名依据 | |||
| 商标名 | GZcosmetics | 通用名 | 滋润保湿面 |
| 属性名 | 霜 | 后缀: | / |
| 命名依据 | 1.“GZcosmetics”为商标名,是注册商标,“GZ”指广州,cosmetics指化妆品,商标总体表达该化妆品品牌源自广州美都。 2.“滋润保湿面”为通用名,指产品具有滋润、保湿的功效,作用部位为面部; 3.“霜”为属性名,表示物理形态为不易流动的霜状产品。 | ||
注:“GZcosmetics”仅为举例,不代表实际注册商标。
问:如何填报化妆品原料的安全相关信息?
答:根据国家药监局《化妆品原料安全信息登记平台上线通知》,普通化妆品备案人可选择以下方式填报原料安全相关信息:(1)通过化妆品注册备案信息服务平台内的原料信息维护模块填报原料安全相关信息;(2)原料生产商或其授权企业已在国家药监局化妆品原料安全信息登记平台报送化妆品原料安全相关信息的,普通化妆品备案人可填写原料报送码关联原料安全信息文件。化妆品备案原料信息填报要求见附件1。
问:如何在化妆品原料安全信息登记平台报送化妆品原料安全相关信息?
答:境内用户直接通过国家药监局网上办事大厅(https://zwfw.nmpa.gov.cn)的“化妆品原料安全信息登记平台”模块进行登陆化妆品原料安全信息登记平台进行填报化妆品原料安全相关信息;境外用户需在“化妆品原料安全信息登记平台”(http://ciip.nifdc.org.cn)开通账号后登陆化妆品原料安全信息登记平台填报化妆品原料安全相关信息。
问:原料安全相关信息包括哪些内容?
答:原料安全相关信息应当包括原料商品名、原料基本信息、原料生产工艺简述、必要的质量控制要求、国际权威机构评估结论、风险物质限制要求等,具体内容见附件2。
问:如何定义原料生产商?原料经销商是否可通过化妆品原料安全信息登记平台报送化妆品原料安全相关信息?
答:原料生产商是指对原料安全承担责任的企业,可以是原料的实际生产企业、与原料实际生产企业隶属同一集团公司的关联企业或者原料委托生产行为中的委托企业。原料经销商根据实际情况判断是否符合原料生产商定义。
原料经销商若同时为原料生产商,则可自行报送化妆品原料安全信息;若非原料生产商,则可作为被授权企业,在提交化妆品原料生产商出具的授权书后,开通化妆品原料安全信息报送权限。
问:着色剂在化妆品备案管理系统应如何填报?标签应如何标注?
答:使用着色剂的,应当在系统“产品配方”原料名称栏标明《化妆品安全技术规范》载明的CI号,产品标签上标注CI号,无CI号的除外。既能做着色剂,又能以其他目的使用的成分,如二氧化钛、云母、氧化锌等,其用作其他使用目的时,系统“产品配方”原料名称及标签标注应为标准中文名称。
附件1
化妆品备案原料信息填报要求
| 序号 | 适用范围 | 原料类别 | 化妆品注册备案信息服务平台填报要求 |
| 1 | 2021.5.1起新备案化妆品 | 所有配方原料 | 填报原料来源、商品名。 |
| 2 | 《化妆品安全技术规范》有质量规格要求的原料,如聚丙烯酰胺类、三乙醇胺、椰油酰胺DEA等。 | 填报原料质量规格或原料安全相关信息。 | |
| 3 | 2022.1.1起新备案化妆品 | 防腐、防晒、着色、染发、祛斑美白功能原料 | 填报原料安全相关信息。 |
| 4 | 2023.1.1起新备案化妆品 | 所有配方原料 | 填报原料安全相关信息。 |
| 5 | 2023.5.1前已备案的化妆品 | 所有配方原料 | 补齐全部原料安全相关信息。 |
附件2
原料安全相关信息
【原料商品名、原料基本信息、原料生产工艺简述】
| 原料商品名 | ||||
| 原料组成 (包括复配组分) | 组分 | 组分中文名称 | 组分INCI名称 | 百分比范围 |
| 1 | (组分名称应与已使用的化妆品原料目录内容一致) | |||
| 2 | ||||
| 3 | (组分名称应与已使用的化妆品原料目录内容一致) | |||
| …… | ||||
| 化妆品中建议添加量 | 基于安全或者功效的角度明确原料在化妆品中的建议添加量,在驻留类和淋洗类化妆品中建议添加量有区别的应当分别予以明确。 | |||
| 原料使用限制(如有) | (该原料在化妆品中的使用限制、配伍禁忌、警示用语的标注要求等) | |||
| 原料性状 | (颜色、气味、状态) | |||
| 物理化学性质描述 | ||||
| 生产工艺类型描述 | 应当明确生产工艺类型:物理粉碎;物理压榨;水或者其他种类溶剂提取;化学合成;生物发酵。简要概述搅拌、加热、蒸馏、过滤、干燥、包装等过程。 直接来源于动植物的天然原料,应明确物种信息、拉丁名、提取部位(藻类和大型真菌类参照此要求)。 生物技术来源原料应明确生产所用的基因来源、载体构建、工程菌信息、供体生物、受体生物、修饰微生物等必要信息。 | |||
1 生物技术来源原料包括水解植物成分
(如无法提供原料组成,可不填写,但应当提交相关说明资料)
【质量控制要求】
| 序号 | 指标名称 | 分子式或结构式(如能明确) | CAS号(如能明确) | 测试方法名称 | 定量范围 |
| 1 | |||||
| 2 | |||||
| 3 |
(如无法提供,可不填写,但应当提交相关说明资料)
(对于化学结构明确的单一原料,应提供纯度要求)
(对于化学结构不明确的原料,应提供指标性成分定量要求或总成分、蒸发残留/固形物含量、干燥失重/水分、炽灼残渣、典型物理化学指标等定量要求)
(聚合物类原料应同时明确聚合度以及平均分子量,如有)
(寡肽类原料还应明确氨基酸序列)
1.鉴别方法
(如无法提供,应当提交相关说明资料)
2.定量控制指标/特征性指标检验方法
(与上表中指标一一对应)
(检验方法仅提供方法名称即可)
3.微生物指标(如适用)
【国际权威机构评估结论】
(如有,应当简要说明,并附权威机构名称)
【其他行业使用要求简述】
【风险物质限量要求】(如有)
| 序号 | 风险物质名称 | CAS号 | 限量要求 | 备注 |
| 1 | ||||
| 2 | ||||
| …… |
重金属指标(如适用):
农药残留风险:(仅植物来源原料,如适用)
微生物污染控制情况:(仅生物技术来源原料,如适用)
宿主致病性、毒性成分控制情况:(仅生物技术来源原料,如适用)
【其他需要说明的问题】
问:关于产品标签上宣称不添加(含)XX原料的问题?
答:化妆品中含有的成分,大部分来源于有目的地配方添加,少量是原料本身所带有或残留的技术工艺上不可避免的微量杂质。在成分宣称上不应绝对化、虚假夸大、贬低同类产品。
产品标签上标注不添加(含)酒精、色素、着色剂等已使用化妆品原料的情形:涉嫌暗示不添加(含)该类原料的产品安全性或品质不及未添加(含)的产品,间接地贬低同类产品,因此不宜标注。
产品标签标注不添加(含)激素、抗生素、氢醌等禁用组分的情形:不添加禁用组分属于产品生产的基本要求,不含的说法则过于绝对化,因此不建议以不添加(含)某禁用组分作为产品标签上宣称。
问:关于产品标签中的禁用语的问题?
答:应规避在产品标签上标注或变相标注禁用语,法律规定的必要生产企业信息除外。建议企业不要宣称“XX透皮给药专利技术”、“药用级别包装工艺”、突出标注“药用层孔菌、药用大黄”等涉嫌误导或暗示消费者有相关医疗功效的内容。
问:关于淡化黑眼圈、眼袋的宣称的问题?
答:经查,黑眼圈的类型和形成机理分为三种,分别为:(1)青色黑眼圈,又称血管型黑眼圈,因血液循环不畅导致眼周肌肤泛青,这是最常见的黑眼圈类型;(2)黑色黑眼圈,也称泪沟形黑眼圈,因眼睛浮肿及眼袋松弛在脸上形成阴影,属于松弛型黑眼圈。(3)茶色黑眼圈,眼周色素沉着或肌肤黯沉导致的色素型黑眼圈。
由于黑眼圈是由血液循环不畅、浮肿、色素沉着等生理原因导致,因此非特殊用途化妆品不具备淡化黑眼圈的功效,如产品宣称淡化黑眼圈,属于夸大产品功效宣称的情况。
眼袋是指下睑皮肤、皮下组织、肌肉及眶膈松弛,眶后脂肪肥大,突出形成的袋状突起,根据病因可分为原发性和继发性两大类。同理,非特殊用途化妆品宣称淡化眼袋同属夸大产品功效宣称的情况。
问:关于身体肌肤紧实的宣称问题?
答:使用于腹部、腰部、背部、手部、腿部等身体部位的产品,若同时宣称紧致肌肤、紧实肌肤,涉嫌误导或暗示消费者具有纤体、塑形、减肥等特殊功效,非特殊用途化妆品标签不应标注此类信息。
问:关于产品标签上专利标注的问题?
答:根据《专利标识标注办法》(国家知识产权局令 第六十三号)第五条要求:“标注专利标识的,应当标明下述内容:(一)采用中文标明专利权的类别,例如中国发明专利、中国实用新型专利、中国外观设计专利;(二)国家知识产权局授予专利权的专利号。”根据第七条要求:“专利权被授予前在产品、该产品的包装或者该产品的说明书等材料上进行标注的,应当采用中文标明中国专利申请的类别、专利申请号,并标明“专利申请,尚未授权”字样。”
因此,涉及专利需要标注的信息包括:(1)专利类别(中国发明专利、中国实用新型专利、中国外观设计专利);(2)专利号;(3)“专利申请,尚未授权”(仅专利权未被授予时);(4)专利涉及的原料名称或工艺类别(仅限发明专利或实用新型专利)。
问:关于产品名称或宣称中原料俗称和配方原料标准中文名称的问题?
答:根据国家药品监管总局《化妆品监督管理常见问题解答(二)》关于“化妆品中文名称中使用原料名称时,应当如何管理?使用的原料名称为通俗名或植物全株名称时,有何具体要求?”的回复,“产品名称中使用的原料名称为通俗名称的,该通俗名称应当与产品配方中该原料的标准中文名称具有一致性的对应关系。”
该通俗名称应为行业广泛认可或国际规定俗名,当这种对应关系难以被消费者识别时,应在标签加以适当解释说明,如类蛇毒肽与二肽二氨基丁酰苄基酰胺二乙酸盐、传明酸与凝血酸、蓝铜肽与三肽-1铜等。
问:关于系列号的标注的问题?
答:《化妆品命名规定》第七条规定:商标名、通用名、属性名相同时,其他需要标注的内容可在属性名后加以注明,包括颜色或色号、防晒指数、气味、适用发质、肤质或特定人群等内容。因此,表示产品色号或货号的系列名称应在属性名后加以标注,如产品名称为XX星光灿烂T-018口红、XX流光溢彩C02.Ka眼影、XX护理1号精油、XX保湿Ⅰ号精华液均为系列名称标注不规范的情况。并且,若根据命名顺序一般为商标名、通用名、属性名的要求,则以上T-018、C02.Ka、1号、Ⅰ号等表述应符合通用名规则,不应出现外文字母、汉语拼音、数字、符号等内容。
问:关于植物提取物标注具体使用部位的问题?
答:根据《已使用化妆品原料目录》(2015版)第五点说明,原料名称为“某某植物提取物”形式的,表示该植物全株及其提取物均为已使用原料,使用时应当注明其具体部位。原料名称为“某某植物花/叶/茎提取物”或“某某植物花/叶/藤提取物”形式的,表示该植物的地上部分及其提取物均为已使用原料,使用时应当注明其具体部位。”
其中《已使用化妆品原料目录》中部分原料,虽目录仅有某某植物提取物,而无与之对应的某某植物根提取物或某某植物叶提取物等,如白薇(CYNANCHUM ATRATUM)提取物、白扁豆(DOLICHOS LABLAB)提取物、白丁香(SYRINGA OBLATA AFFINIS)提取物等,此类原料表示该原料的全株及其提取物均为已使用原料,使用时同样应注明其具体部位。
问:关于原液、纯露属性名的问题
答:原液一般指单一组分或单一类别组分为功效成分,与必需的溶剂、抗氧化剂、防腐剂混合而成,直接使用或按规定比例稀释后使用,起护理作用的液态化妆品。
纯露,又称水精油,是指精油在蒸馏萃取过程中,在提炼精油时分离出来的一种100%饱和的蒸馏原液。
企业应根据产品配方特点确定产品实际属性名。
问:注册商标说明问题?
答:根据《化妆品命名规定》第五条的规定“注册商标以及必须使用外文字母、符号的需在说明书中用中文说明,但约定俗成、习惯使用的除外,如维生素C。”如果有非中文注册商标用作产品商标名,标签有Ⓡ标记并在相邻位置有对应中文,则无需再另行解释说明;如果没有Ⓡ标记或没有对应中文,则需要另行解释说明;字母、图案等无具体含义的注册商标名规范注解为“仅为注册商标,无含义”。
问:名称规范问题?
答:根据《化妆品命名规定》第三条第二款和第三款的要求,化妆品命名必须符合“(二)简明、易懂,符合中文语言习惯;(三)不得误导、欺骗消费者。”的基本原则,以下情况产品名称有异议的,需要进一步解释说明:(1)“古方”“汉方”“苗方”等作为产品商标名,需要在标签中解释说明“仅作为商标名,不具备药物功效”;“杏林”等作为产品商标名,需要在标签中解释说明“仅作为商标名,不作医学词意理解”等。(2)“花婴堂”作为商标名,易使消费者误解为婴幼儿产品,如实际不是婴幼儿产品需要在标签中解释说明。
问:包装图片上传要求?
答:根据《关于调整化妆品注册备案管理有关事宜的通告》(2013年第10号)要求,应当按要求通过统一的网络平台报送产品销售包装。在报送的立体图和平面图中,如立体图是实际市售包装图,平面图可以是设计图或者效果图;立体图是设计图或者效果图,则平面图应当是实际市售包装图。产品标签的设计图和效果图应与产品销售包装一致,且产品立体图应能体现包装立体效果。
问:配方填报和成分标注问题?
答:如配方中同一物质重复填报,应当做质量规格说明(复配原料除外)。产品成分以复配方式填报的,应将其中各组分的加入量进行换算后,与配方中相同的组分相加,再在标签进行排序。
问:化妆品标签标注GMPC、ISO等质量管理体系认证标志的问题?
答:根据《中华人民共和国认证认可条例》第二十五条的要求:“获得认证证书的,应当在认证范围内使用认证证书和认证标志,不得利用产品、服务认证证书、认证标志和相关文字、符号,误导公众认为其管理体系已通过认证,也不得利用管理体系认证证书、认证标志和相关文字、符号,误导公众认为其产品、服务已通过认证。”因此,不宜在化妆品标签上标注GMPC、ISO等质量管理体系认证标志,涉嫌误导公众认为其产品已通过认证。
问:关于商标注册证使用问题?
答:根据《中华人民共和国商标法》第二十三条及第五十六条的规定:“注册商标需要在核定使用范围之外的商品上取得商标专用权的,应当另行提出注册申请”、“注册商标的专用权,以核准注册的商标和核定使用的商品为限”。因此,企业应在注册商标的核定使用范围之内享受商标专用权,注册商标的核定使用范围应包含申报备案产品。
另根据《化妆品命名规定》第六条的要求:“商标名应当符合本规定的相关要求。”商标名的使用除符合国家商标有关法律法规的规定外,还应当符合国家化妆品管理相关法律法规的规定,不得以商标名的形式宣称医疗效果或产品不具备的功效。
问:关于产品包装上传问题?
答:根据《关于调整化妆品注册备案管理有关事宜的通告》(2013年第十号文)的要求,企业应当按要求通过统一的网络平台报送产品销售包装(含产品标签、产品说明书)至所在地行政区域内的省级食品药品监管部门。为保证上传包装图片为销售包装,不建议以粘贴、剪切、涂改等方式对产品原标签相关内容进行修改或者补充。为方便企业实际工作,上传平面图可以为设计稿或效果图,但立体图必须为销售包装实图。
问:关于GB 29680《洗面奶、洗面膏》标准分类型号标注问题?
答:根据洗面奶、洗面膏产品的工艺不同,可分为乳化型(Ⅰ型)、非乳化型(Ⅱ型)。乳化型洗面奶的定义为“由水、油两相原料经少量表面活性剂乳化制得的洗面奶”;乳化型洗面膏的定义为“由水、油两相原料经少量表面活性剂乳化制得的洗面膏”。非乳化型洗面奶定义为“主要以表面活性剂包括脂肪酸盐类,经复配其他原料混合制得的洗面奶”;非乳化型洗面膏的定义为“主要以表面活性剂包括脂肪酸盐类,经复配其他原料混合制得的洗面膏”。企业应根据产品工艺类型及原料配比准确标示洗面奶(膏)的分类型号。
问:关于标签宣称问题?
答:根据《化妆品标识管理规定》的要求:“化妆品标识应当真实、准确、科学、合法”、“不得标注夸大功能、虚假宣传、贬低同类产品的内容”。
(1)经查光甘草定与光果甘草(GLYCYRRHIZA GLABRA)根、光果甘草(GLYCYRRHIZA GLABRA)根提取物、光果甘草(GLYCYRRHIZA GLABRA)提取物等原料均不是一致性的对应关系,且光甘草定位未收纳于《已使用化妆品原料目录》(2015版)中,不宜宣称光甘草定;
(2)标签宣称“食品级原料“易将食品与化妆品混淆,不宜宣称。
问:儿童化妆品标志对字体和颜色的要求是否必须与公告中建议的字体、颜色一致?
答:根据《儿童化妆品监督管理规定》,儿童化妆品应当在在销售包装展示面标注儿童化妆品标志。为便于消费者识别,儿童化妆品标志应当等比例标注在销售包装主要展示面的左上方,清晰易识别。儿童化妆品标志整体采用金色,对公告中的配色信息不做强制要求,儿童化妆品企业可根据实际包装情况,对颜色和字体进行微调,但应当清晰、持久,易于辨认、识读。
问:若化妆品标签存在《办法》第二十条规定的瑕疵,企业可以采取哪些改正措施?
答:化妆品标签存在瑕疵但不影响质量安全且不会对消费者造成误导的,企业应当及时予以改正,可以重新印制标签,也可以通过粘贴覆盖的形式对瑕疵进行改正,但改正后的标签应当清晰、持久,易于辨认、识读,不得有印字脱落、粘贴不牢等现象。
问:化妆品原料中添加的如抗氧化剂、防腐剂、稳定剂等保护原料的成分,是否应当在产品标签上进行标注?
答:《办法》规定化妆品标签应当在销售包装可视面标注化妆品全部成分的原料标准中文名称。化妆品成分是指生产过程中有目的地添加到产品配方中,并在最终产品中起到一定作用的成分。为了保证化妆品原料质量而在原料中添加的极其微量的抗氧化剂、防腐剂、稳定剂等成分,虽然在申请注册或者进行备案时以该原料复配的形式进行产品配方填报,但不属于化妆品的成分,可以不在产品标签上进行标注;当然企业为保障消费者知情权,也可以在产品标签进行标注。
问:化妆品名称中的通用名使用具体原料名称或者表明原料类别的词汇的,有何要求?
答:《办法》规定使用具体原料名称或者表明原料类别的词汇的,应当与产品配方成分相符,且该原料在产品中产生的功效作用应当与产品功效宣称相符,如产品名称为“某某氨基酸面膜”,产品功效宣称为抗皱,则产品配方中应包含氨基酸,并且氨基酸的使用目的应当与抗皱相关。使用动物、植物或者矿物等名称描述产品的香型、颜色或者形状的,配方中可以不含此原料,命名时可以在通用名中采用动物、植物或者矿物等名称加香型、颜色或者形状的形式,也可以在属性名后加后缀注明,如黄瓜味洗面奶或者洗面奶(黄瓜味)。
问:化妆品配方中存在含量不超过0.1%(w/w)的成分,如何标注?
答:根据《办法》规定,微量成分是指化妆品配方中含量不超过0.1%(w/w)的成分,当产品配方中含有微量成分时,应当以“其他微量成分”作为引导语引出另行标注,可以不按照成分含量的降序列出。微量成分只需标注一次,在“成分”引导语后不再进行重复标注。
问:化妆品生产企业(含自行生产的注册人、备案人及受托生产企业)若注册地址和实际生产地址不一致,如何标注生产企业地址?
答:根据《化妆品监督管理条例》(以下称《条例》)《办法》规定,化妆品标签应当标注注册人、备案人、受托生产企业的名称、地址。若注册地址和实际生产地址不一致,应当标注生产许可证上载明的实际生产地址。
问:申请特殊化妆品注册,在化妆品智慧申报审评系统中如何填报防晒类化妆品《注册申请表》中的SPF值、浴后SPF值以及PA等级?
答:填报时,《注册申请表》中的SPF值、浴后SPF值以及PA等级应当与产品中文名称、产品标签样稿中标注的SPF值等信息一致。
问:特殊化妆品填报《注册申请表》分类编码时,注册人或者境内责任人应当注意什么?
答:应当根据《化妆品分类规则和分类目录》等相关法规要求,正确规范填报《注册申请表》分类编码,避免遗漏或者填写错误。申报资料中相关内容应当与所填报的分类编码相符,如产品标签样稿中功效宣称、使用方法、作用部位、适用人群等内容应当与分类编码相符;含推进剂的,产品剂型应当包括“气雾剂”;使用人群包括“婴幼儿”“儿童”的,应当遵循儿童化妆品的相关规定等。
问:对香精如何进行安全评估?
答:香精为类别原料,不可使用《已使用化妆品原料目录(2021年版)》中“香精”最高历史使用量作为评估证据,应按照《化妆品安全评估技术导则》的原则和要求对香精进行评估,或提供产品所用香精符合国际日用香料协会(IFRA)实践法规要求或符合我国相关(香精)国家标准的证明文件。
问:对配方中使用的纳米原料进行评估时,应提供哪些相关资料?
答:对产品配方中含有纳米原料的产品进行安全评估时,应提供原料生产商出具的原料质量规格,并提供基于该原料的质量规格和支持配方使用量的安全评估资料。
问:配方中含有纳米原料,配方表中应当如何标注?
答:应按照《化妆品注册备案资料管理规定》要求,在纳米原料名称后标注“(纳米级)”。
问:使用贴、膜类载体材料的产品,应当如何填报?
答:应勾选配方表下“是否膜质载体材料”选项,并按照《化妆品注册备案资料管理规定》要求备注说明主要载体材料的材质组成,同时提供其来源、制备工艺、质量控制指标等资料。
问:产品配方含有与产品内容物直接接触的推进剂的,应当如何进行推进剂的填报?
答:应按照《化妆品注册备案资料管理规定》要求,在配方表下方作推进剂相关信息的单独填报,推进剂含量合计应为100%。
问:化妆品智慧申报审评系统中生产工艺中原料分相信息应如何填报?
答:应在生产工艺“分相信息”模块项下,进行原料分相信息的填报;无需在生产工艺“步骤”、“备注”栏中重复填报分相相关内容。
问:注册人被吸收合并或成立子公司,可以申请变更注册人吗?
答:根据《化妆品注册备案管理办法》第四十九条规定,化妆品注册证不得转让。因企业合并、分立等法定事由导致原注册人主体资格注销,将注册人变更为新设立的企业或者其他组织的,应当按照本办法的规定申请变更注册。
问:多个进口产品列在了同一生产销售证明上,每个产品都需提交销售证明原件吗?如果提交了复印件还需要公证吗?
答:根据《化妆品注册备案资料管理规定》第二十七条,进口产品的已上市销售证明文件、委托关系文件或者属于一个集团公司的证明资料等文件可同时列明多个产品。这些产品申请注册或者办理备案时,其中一个产品可使用原件,其他产品可使用复印件,并说明原件所在的产品名称以及相关受理编号、注册证号或者备案编号等信息。
问:多色号系列进口普通化妆品按《化妆品注册和备案检验工作规范》抽样进行毒理学试验的,可以使用毒理学实验报告的复印件吗?
答:可以使用复印件。根据《化妆品注册备案资料管理规定》第三十三条,多色号系列普通化妆品按《化妆品注册和备案检验工作规范》抽样进行毒理学试验的,可作为一组产品进行备案,每个产品均应附上系列产品的名单、基础配方和着色剂一览表以及抽检产品名单。
问:进口普通化妆品注销后再次备案时可以使用原备案资料的复印件吗?
答:根据《化妆品注册备案资料管理规定》第五十九条,普通产品注销后再次备案时,应当提交情况说明。对于非安全性原因注销的,再次申请备案时可使用原备案资料的复印件。
问:特殊化妆品不予注册, 再次申报资料的要求是什么,可以使用复印件吗?
答:根据《化妆品注册备案资料管理规定》第五十八条,对于非安全性原因不予注册的特殊产品再次申请注册时,可使用原注册资料的复印件,同时提交不予注册未涉及安全性的说明,包括对不予注册原因的解释。
问:境外用户注册化妆品原料安全信息登记平台所需企业主体证明文件有什么要求?
答:企业主体证明文件应由中国公证机关公证或由我国使(领)馆确认;文本为外文的均应完整、规范地翻译为中文,并将原文附在相应的译文之后。
问:化妆品新原料可以授权多个境内责任人吗?
答:根据《化妆品新原料注册备案资料管理规定》第十一条规定,同一化妆品新原料不得授权多个境内责任人。
问:化妆品原料安全信息登记平台如何登录,是否需要注册账户?
答:境内用户不需要注册账户,可直接通过国家药监局网上办事大厅(https://zwfw.nmpa.gov.cn)的“化妆品原料安全信息登记平台”模块进行登陆;境外用户需在“化妆品原料安全信息登记平台”(http://ciip.nifdc.org.cn)注册,上传经由中国公证机关公证或由我国使(领)馆确认的企业主体证明文件,审核通过后登陆。
问:新原料境内责任人授权书到期了怎么办?
答:根据《化妆品新原料注册备案资料管理规定》第十一条规定,境内责任人授权书所载明的授权期限到期后,应当在授权期限届满前30日内重新提交延长授权期限的授权书或按要求办理境内责任人变更。
问:新原料用户名申请时境内责任人授权书应写明哪些内容?
答:根据《化妆品新原料注册备案资料管理规定》第十一条规定,境内责任人授权书应当至少载明以下内容和信息:化妆品新原料注册人、备案人和境内责任人名称;授权和被授权关系;授权范围;授权期限。


